
Versione del 24 febbraio 2021
Sommario
1.IL CONTESTO
2.RIFERIMENTI NORMATIVI PRINCIPALI
2.1.DISPOSITIVO DELL'ART. 2087 CODICE CIVILE
2.2.ART. 32 COSTITUZIONE ITALIANA
2.3.DECRETO LEGISLATIVO N° 81, 9 APRILE 2008, ART. 279, PREVENZIONE E CONTROLLO
2.4.PROTOCOLLO CONDIVISO DI REGOLAMENTAZIONE DELLE MISURE PER IL CONTRASTO E IL CONTENIMENTO DELLA DIFFUSIONE DEL VIRUS COVID-19 NEGLI AMBIENTI DI LAVORO
3.LA VALUTAZIONE DEL RISCHIO: DVR, DOCUMENTO DI VALUTAZIONE DEI RISCHI (ART. 18 DEL D.LGS. 81/08 E S.M.I.)
3.1.IL RUOLO DEGLI RLS (RAPPRESENTANTI DEI LAVORATORI PER LA SICUREZZA)
3.2.DECRETO LEGISLATIVO N° 81, 9 APRILE 2008, ARTICOLO 28 - OGGETTO DELLA VALUTAZIONE DEI RISCHI
3.3.DECRETO LEGISLATIVO N° 81, 9 APRILE 2008, ARTICOLO 271 - VALUTAZIONE DEL RISCHIO
3.4.DECRETO LEGISLATIVO N° 81, 9 APRILE 2008, ARTICOLO 20 – OBBLIGHI DEI LAVORATORI
4.CONSIDERAZIONI GENERALI INERENTI ALLA MEDICINA DEL LAVORO
4.1.LE NOVITÀ NORMATIVE IN TERMINI DI LIVELLO DI RISCHIO DELL’AGENTE PATOGENO SARS-COV-2
4.2.ATTIVITÀ GIÀ SOGGETTE A RISCHIO BIOLOGICO (ES. ATTIVITÀ SANITARIE E SOCIO-SANITARIE)
5.IL RISCHIO SPECIFICO IN AMBITO SANITARIO
6.INFORMAZIONI SUL FARMACO
6.1.DIRITTO ALL’INFORMAZIONE
6.2.COMIRNATY È UN VACCINO?
6.3.COPERTURA IMMUNITARIA ED EFFICACIA di COMIRNATY
6.4.QUESITI APERTI
7.RISCHI COLLEGATI ALLA PROPOSTA DI SOMMINISTRAZIONE DI COMIRNATY
7.1.RISCHI COLLEGATI ALLA AUTORIZZAZIONE ALL'IMMISSIONE IN COMMERCIO CONDIZIONATA (CMA, CONDITIONAL MARKETING APPROVAL)
7.2.RISCHI COLLEGATI ALL’IMPIEGO DELLA TECNOLOGIA mRNA
7.3.RISCHIO COLLEGATO A UNA PRECEDENTE DIAGNOSI DI POSITIVITA' A COVID-19
7.4.RISCHI IDENTIFICATI, RISCHI POTENZIALI E INFORMAZIONI MANCANTI
7.5.QUESITI APERTI
8.CONSIDERAZIONI SULLA VALUTAZIONE DEL RISCHIO
8.1.LETALITA’ E MORTALITA’
8.2.DISTRIBUZIONE DELLA GRAVITA' DEI CASI DI COVID-19
8.3.L'ANDAMENTO DELLA MORTALITA' NEGLI ULTIMI ANNI
9.I TRATTAMENTI POSSIBILI DEL COVID-19
9.1.QUESITI APERTI
1. IL CONTESTO
Il presente documento intende orientare alla gestionedelle possibili vertenze nei luoghi di lavoro derivanti dalle richieste di vaccinazione (obbligatoria) con i vaccini Covid-19 disponibili.
Tutto il mondo del lavoro è interessato da questo fenomeno che è particolarmente acuito dalla permanenza di uno stato di emergenza. I lavoratori che stanno vivendo le difficoltà maggiori sono quelli del comparto sanitario, medici, infermieri OSS.
La Circolare del Ministero della salute del 24.12.20201, detta le raccomandazioni per l’organizzazione della campagna vaccinale contro SARS-CoV-2/Covid-19 e procedure di vaccinazione.
Si precisa che attualmente gli unici vaccini autorizzati all’immissione in commercio condizionata (CMA) sono:
- Comirnaty (nome nella sperimentazione: BNT162b2; nome generico: tozinameran) di Pzfizer- BioNTech;
- Moderna COVID-19 Vaccine (nome nella sperimentazione: mRNA-1273; nome generico CX-024414; altri nomi: COVID-19 Vaccine Moderna, COVID-19 mRNA Vaccine Moderna) di Moderna;
- COVID-19 Vaccine AstraZeneca (nome nella sperimentazione: ChAdOx1 nCoV-19 vaccine (AZD1222)) di Oxford University e AstraZeneca.
Per quanto qui di interesse la citata circolare chiarisce anzitutto le “Categorie Target” indentificate, vista la scarsità di dosi vaccinali a disposizione, in operatori sanitari e sociosanitari; personale e ospiti dei presidi residenziali per anziani (RSA)
Il settore sanitario pubblico e privato è dunque il target iniziale e quello dal quale stiamo in effetti ricevendo le prime richieste di assistenza.
La circolare fornisce in allegato anche il Modulo di consenso informato che dovrà essere sottoposto al momento della vaccinazione, redatto dall’Osservatorio per le buone pratiche sulla sicurezza nella sanità presso Age. Na.S. (Agenzia Nazione per i Servizi Sanitari).
Il modulo di Consenso Informato è contenuto nella Circolare del Ministero della salute del 24.12.2020 come allegato.
Il Ministero della Salute chiarisce inoltre che, per la somministrazione del vaccino anti Covid-19 sono stati identificati i seguenti Punti Vaccinali:
- Punto vaccinale Ospedaliero (PVO)
- Punto Vaccinale Territoriale (PVT)
- Punto Vaccinale in Struttura Residenziale (PVSR)
Appare evidente che i Punti Vaccinali coincidono con i Datori di Lavoro del Target di riferimento (operatori sanitari e sociosanitari e personale di RSA) e quindi, in ragione delle possibili e paventate conseguenze del rifiuto della vaccinazione sul rapporto lavoro - demansionamento, sospensione della mansione, licenziamento ecc. - è importante gestire adeguatamente il cosiddetto “rifiuto alla vaccinazione” e, in caso di dubbi, mettere in contatto il lavoratore con l’assistenza legale.
2.RIFERIMENTI NORMATIVI PRINCIPALI
2.1. DISPOSITIVO DELL'ART. 2087 CODICE CIVILE
L'imprenditore è tenuto ad adottare nell'esercizio dell'impresa le misure che, secondo la particolarità del lavoro, l'esperienza e la tecnica, sono necessarie a tutelare l'integrità fisica e la personalità morale dei prestatori di lavoro [Cost. 37, 41]2.
2.2. ART. 32 COSTITUZIONE ITALIANA
La Repubblica tutela la salute come fondamentale diritto dell'individuo e interesse della collettività, e garantisce cure gratuite agli indigenti.
Nessuno può essere obbligato a un determinato trattamento sanitario se non per disposizione di legge. La legge non può in nessun caso violare i limiti imposti dal rispetto della persona umana.
2.3. DECRETO LEGISLATIVO N° 81, 9 APRILE 2008, ART. 279, PREVENZIONE E CONTROLLO
1. I lavoratori addetti alle attività per le quali la valutazione dei rischi ha evidenziato un rischio per la salute sono sottoposti alla sorveglianza sanitaria.
2. Il datore di lavoro, su conforme parere del medico competente, adotta misure protettive particolari per quei lavoratori per i quali, anche per motivi sanitari individuali, si richiedono misure speciali di protezione, fra le quali:
a) la messa a disposizione di vaccini efficaci per quei lavoratori che non sono già immuni all'agente biologico presente nella lavorazione, da somministrare a cura del medico competente;
b) l'allontanamento temporaneo del lavoratore secondo le procedure dell'articolo 42.
3. Ove gli accertamenti sanitari abbiano evidenziato, nei lavoratori esposti in modo analogo ad uno stesso agente, l'esistenza di anomalia imputabile a tale esposizione, il medico competente ne informa il datore di lavoro.
4. A seguito dell'informazione di cui al comma 3 il datore di lavoro effettua una nuova valutazione del rischio in conformità all'articolo 271.
5. Il medico competente fornisce ai lavoratori adeguate informazioni sul controllo sanitario cui sono sottoposti e sulla necessità di sottoporsi ad accertamenti sanitari anche dopo la cessazione dell'attività che comporta rischio di esposizione a particolari agenti biologici individuati nell'allegato XLVI nonché sui vantaggi ed inconvenienti della vaccinazione e della non vaccinazione.
Fermo quanto sopra, ai sensi del D.Lgs. 81/2008, la sorveglianza sanitaria all’interno dei luoghi di lavoro è di esclusiva competenza del medico competente, al quale spetta in via esclusiva il giudizio di idoneità – totale, parziale, temporanea, permanente – alla mansione;
- ai sensi dell’art.279 del predetto decreto, sempre dopo parere del medico competente, è prevista semmai la messa a disposizione di vaccini efficaci;
- in assenza di un obbligo la comunicazione di dati sanitari, quale l’avvenuta effettuazione della profilassi vaccinale, corrisponde ad una violazione delle norme sulla protezione dei dati personali.
2.4. PROTOCOLLO CONDIVISO DI REGOLAMENTAZIONE DELLE MISURE PER IL CONTRASTO E IL CONTENIMENTO DELLA DIFFUSIONE DEL VIRUS COVID-19 NEGLI AMBIENTI DI LAVORO3
Riportiamo di seguito alcuni passaggi fondamentali di questo documento.
Il documento, tenuto conto dei vari provvedimenti del Governo e, da ultimo, del DPCM 10 aprile 2020, nonché di quanto emanato dal Ministero della Salute, contiene linee guida condivise tra le Parti per agevolare le imprese nell’adozione di protocolli di sicurezza anti-contagio, ovverosia Protocollo di regolamentazione per il contrasto e il contenimento della diffusione del virus COVID 19 negli ambienti di lavoro.
La prosecuzione delle attività produttive può infatti avvenire solo in presenza di condizioni che assicurino alle persone che lavorano adeguati livelli di protezione. La mancata attuazione del Protocollo che non assicuri adeguati livelli di protezione determina la sospensione dell’attività fino al ripristino delle condizioni di sicurezza.
…
L’obiettivo del presente protocollo condiviso di regolamentazione è fornire indicazioni operative finalizzate a incrementare, negli ambienti di lavoro non sanitari, l’efficacia delle misure precauzionali di contenimento adottate per contrastare l’epidemia di COVID-19.
Il COVID-19 rappresenta un rischio biologico generico, per il quale occorre adottare misure uguali per tutta la popolazione. Il presente protocollo contiene, quindi, misure che seguono la logica della precauzione e seguono e attuano le prescrizioni del legislatore e le indicazioni dell’Autorità sanitaria.
…
1-INFORMAZIONE
L’azienda, attraverso le modalità più idonee ed efficaci, informa tutti i lavoratori e chiunque entri in azienda circa le disposizioni delle Autorità, consegnando e/o affiggendo all’ingresso e nei luoghi maggiormente visibili dei locali aziendali, appositi depliants informativi, in particolare contenenti:
- l’obbligo di rimanere al proprio domicilio in presenza di febbre (oltre 37.5°) o altri sintomi influenzali e di chiamare il proprio medico di famiglia e l’autorità sanitaria
- la consapevolezza e l’accettazione del fatto di non poter fare ingresso o di poter permanere in azienda e di doverlo dichiarare tempestivamente laddove, anche successivamente all’ingresso, sussistano le condizioni di pericolo (sintomi di influenza, temperatura, provenienza da zone a rischio o contatto con persone positive al virus nei 14 giorni precedenti, etc) in cui i provvedimenti dell’Autorità impongono di informare il medico di famiglia e l’Autorità sanitaria e di rimanere al proprio domicilio
- l’impegno a rispettare tutte le disposizioni delle Autorità e del datore di lavoro nel fare accesso in azienda (in particolare, mantenere la distanza di sicurezza, osservare le regole di igiene delle mani e tenere comportamenti corretti sul piano dell’igiene)
- l’impegno a informare tempestivamente e responsabilmente il datore di lavoro della presenza di qualsiasi sintomo influenzale durante l’espletamento della prestazione lavorativa, avendo cura di rimanere ad adeguata distanza dalle persone presenti
L’azienda fornisce una informazione adeguata sulla base delle mansioni e dei contesti lavorativi, con particolare riferimento al complesso delle misure adottate cui il personale deve attenersi in particolare sul corretto utilizzo dei DPI per contribuire a prevenire ogni possibile forma di diffusione di contagio.
…
5-PRECAUZIONI IGIENICHE PERSONALI
- è obbligatorio che le persone presenti in azienda adottino tutte le precauzioni igieniche, in particolare per le mani
- l’azienda mette a disposizione idonei mezzi detergenti per le mani
- è raccomandata la frequente pulizia delle mani con acqua e sapone
- I detergenti per le mani di cui sopra devono essere accessibili a tutti i lavoratori anche grazie a specifici dispenser collocati in punti facilmente individuabili.
6-DISPOSITIVI DI PROTEZIONE INDIVIDUALE
- l’adozione delle misure di igiene e dei dispositivi di protezione individuale indicati nel presente Protocollo di Regolamentazione è fondamentale e, vista l’attuale situazione di emergenza, è evidentemente legata alla disponibilità in commercio. Per questi motivi:
a. le mascherine dovranno essere utilizzate in conformità a quanto previsto dalle indicazioni dell’Organizzazione mondiale della sanità.
b. data la situazione di emergenza, in caso di difficoltà di approvvigionamento e alla sola finalità di evitare la diffusione del virus, potranno essere utilizzate mascherine la cui tipologia corrisponda alle indicazioni dall’autorità sanitari.
c. è favorita la preparazione da parte dell’azienda del liquido detergente secondo le indicazioni dell’OMS (https://www.who.int/gpsc/5may/Guide_to_Local_Production.pdf)
d. qualora il lavoro imponga di lavorare a distanza interpersonale minore di un metro e non siano possibili altre soluzioni organizzative è comunque necessario l’uso delle mascherine, e altri dispositivi di protezione (guanti, occhiali, tute, cuffie, camici, ecc.) conformi alle disposizioni delle autorità scientifiche e sanitarie.
- nella declinazione delle misure del Protocollo all’interno dei luoghi di lavoro sulla base del complesso dei rischi valutati e, a partire dalla mappatura delle diverse attività dell’azienda, si adotteranno i DPI idonei. E’ previsto, per tutti i lavoratori che condividono spazi comuni, l’utilizzo di una mascherina chirurgica, come del resto normato dal DL n. 9 (art. 34) in combinato con il DL n. 18 (art 16 c. 1)
…
12-SORVEGLIANZA SANITARIA/MEDICO COMPETENTE/RLS
- La sorveglianza sanitaria deve proseguire rispettando le misure igieniche contenute nelle indicazioni del Ministero della Salute (cd. decalogo)
- vanno privilegiate, in questo periodo, le visite preventive, le visite a richiesta e le visite da rientro da malattia
- la sorveglianza sanitaria periodica non va interrotta, perché rappresenta una ulteriore misura di prevenzione di carattere generale: sia perché può intercettare possibili casi e sintomi sospetti del contagio, sia per l’informazione e la formazione che il medico competente può fornire ai lavoratori per evitare la diffusione del contagio
- nell’integrare e proporre tutte le misure di regolamentazione legate al COVID-19 il medico competente collabora con il datore di lavoro e le RLS/RLST.
- Il medico competente segnala all’azienda situazioni di particolare fragilità e patologie attuali o pregresse dei dipendenti e l’azienda provvede alla loro tutela nel rispetto della privacy.
- Il medico competente applicherà le indicazioni delle Autorità Sanitarie. Il medico competente, in considerazione del suo ruolo nella valutazione dei rischi e nella sorveglia sanitaria, potrà suggerire l’adozione di eventuali mezzi diagnostici qualora ritenuti utili al fine del contenimento della diffusione del virus e della salute dei lavoratori.
- Alla ripresa delle attività, è opportuno che sia coinvolto il medico competente per le identificazioni dei soggetti con particolari situazioni di fragilità e per il reinserimento lavorativo di soggetti con pregressa infezione da COVID 19.
E’ raccomandabile che la sorveglianza sanitaria ponga particolare attenzione ai soggetti fragili anche in relazione all’età
Per il reintegro progressivo di lavoratori dopo l’infezione da COVID19, il medico competente, previa presentazione di certificazione di avvenuta negativizzazione del tampone secondo le modalità previste e rilasciata dal dipartimento di prevenzione territoriale di competenza, effettua la visita medica precedente alla ripresa del lavoro, a seguito di assenza per motivi di salute di durata superiore ai sessanta giorni continuativi, al fine di verificare l’idoneità alla mansione”. (D.Lgs 81/08 e s.m.i, art. 41, c. 2 lett. e-ter), anche per valutare profili specifici di rischiosità e comunque indipendentemente dalla durata dell’assenza per malattia.
3. LA VALUTAZIONE DEL RISCHIO: DVR, DOCUMENTO DI VALUTAZIONE DEI RISCHI (ART. 18 DEL D.LGS. 81/08 E S.M.I.)
Il Documento di Valutazione dei Rischi (DVR) è quel documento che la legge sulla sicurezza nei luoghi di lavoro ha imposto a tutte le aziende con almeno un lavoratore, anche socio, come mezzo per garantire la sicurezza nei luoghi di lavoro e dimostrare agli organi di controllo l'avvenuta Valutazione dei Rischi per tutelare la salute dei lavoratori.
Si tratta, quindi, di un documento obbligatorio che deve essere conservato presso la sede dell'azienda e serve principalmente a delineare tutti gli interventi che devono essere attuati per eliminare o ridurre i rischi e pericoli presenti all'interno dei luoghi di lavoro. Per la sua redazione è necessario analizzare la struttura aziendale e le attività operative al fine di individuare i rischi e valutare i pericoli che gravano sulla sicurezza interna.
La sua predisposizione, in conformità a quanto previsto dalla norma, prevede:
- descrizione dei luoghi di lavoro, delle attività esercitate, delle attrezzature e macchinari, del personale presente e delle relative mansioni;
- individuazione dei fattori di pericolo sui luoghi di lavoro, analisi e valutazione dei rischi connessi;
- analisi e valutazione dei rischi operativi;
- elaborazione di apposite schede di valutazione dei rischi collegati alle mansioni;
- definizione del programma degli interventi di adeguamento e/o miglioramento necessari.
- Mantenimento del documento DVR aggiornato in base ai cambiamenti aziendali e/o legislativi.
3.1. IL RUOLO DEGLI RLS (RAPPRESENTANTI DEI LAVORATORI PER LA SICUREZZA)
Ai sensi del D.Lgs. 81/08 la consultazione degli RLS è prevista nei seguenti casi:
“Articolo 19” n. 2/2015: la consultazione dei Rls
Nel D.Lgs 81/2008 e successive modifiche ed integrazioni viene spesso riproposto il tema della consultazione, ovvero di quel processo con cui il datore di lavoro deve acquisire il parere dei RLS nel merito di alcune delle sue attività e scelte. La consultazione è obbligatoria, ma non vincolante. Il datore di lavoro è infatti obbligato a “consultare” i RLS per conoscere il loro parere ma può decidere in piena autonomia e piena responsabilità.
Quando il D. Lgs 81/2008 prevede la consultazione dei RLS
I casi specifici sono previsti nel Titolo I (Principi comuni) del D.Lgs stesso, e sono, in ordine di citazione, i 6 che seguono:
Articolo 15 - Misure generali di tutela. Comma 1
Le misure generali di tutela della salute e della sicurezza dei lavoratori nei luoghi di lavoro sono: voce “s”: “la partecipazione e consultazione dei rappresentanti dei lavoratori per la sicurezza”.
Articolo 18 - Obblighi del datore di lavoro e del dirigente. Comma 1
Il datore di lavoro, che esercita le attività di cui all’articolo 3, e i dirigenti, che organizzano e dirigono le stesse attività secondo le attribuzioni e competenze ad essi conferite, devono: voce s: consultare il rappresentante dei lavoratori per la sicurezza nelle ipotesi di cui all’articolo 50.
Articolo 29 - Modalità di effettuazione della valutazione dei rischi. Comma 2
Le attività di cui al comma 1 [n.b. valutazione dei rischi ed elaborazione del relativo documento] sono realizzate previa consultazione del rappresentante dei lavoratori per la sicurezza.
Articolo 50 - Attribuzioni del rappresentante dei lavoratori per la sicurezza. Comma 1
Fatto salvo quanto stabilito in sede di contrattazione collettiva, il rappresentante dei lavoratori per la sicurezza:
voce b: è consultato preventivamente e tempestivamente in ordine alla valutazione dei rischi, alla individuazione, programmazione, realizzazione e verifica della prevenzione nella azienda o unità produttiva;
voce c: è consultato sulla designazione del responsabile e degli addetti al servizio di prevenzione, alla attività di prevenzione incendi, al primo soccorso, alla evacuazione dei luoghi di lavoro e del medico competente; voce d: è consultato in merito all’organizzazione della formazione di cui all’articolo 37.
Gli RLS devono essere consultati in ordine a quelli che sono i processi più importanti del sistema di prevenzione aziendale: la valutazione dei rischi, l’individuazione, programmazione, realizzazione e verifica delle misure preventive in azienda, la formazione alla sicurezza dei lavoratori, la scelta, da parte del datore di lavoro, delle persone cui affidare i fondamentali ruoli per la sicurezza e tutela della salute in azienda, ovvero RSPP (Responsabile del Servizio di Prevenzione e Protezione), addetti del SPP (Servizio di Prevenzione e Protezione), medico competente, addetti alle emergenze.
3.2.DECRETO LEGISLATIVO N° 81, 9 APRILE 2008, ARTICOLO 28 - OGGETTO DELLA VALUTAZIONE DEI RISCHI
1. La valutazione di cui all'articolo 17, comma 1, lettera a), anche nella scelta delle attrezzature di lavoro e delle sostanze o dei preparati chimici impiegati, nonché nella sistemazione dei luoghi di lavoro, deve riguardare tutti i rischi per la sicurezza e la salute dei lavoratori, ivi compresi quelli riguardanti gruppi di lavoratori esposti a rischi particolari, tra cui anche quelli collegati allo stress lavoro-correlato, secondo i contenuti dell'accordo europeo dell'8 ottobre 2004, e quelli riguardanti le lavoratrici in stato di gravidanza, secondo quanto previsto dal decreto legislativo 26 marzo 2001, n. 151, nonché quelli connessi alle differenze di genere, all'età, alla provenienza da altri Paesi.
2. Il documento di cui all'articolo 17, comma 1, lettera a), redatto a conclusione della valutazione, deve avere data certa e contenere:
a) una relazione sulla valutazione di tutti i rischi per la sicurezza e la salute durante l'attività lavorativa, nella quale siano specificati i criteri adottati per la valutazione stessa;
b) l'indicazione delle misure di prevenzione e di protezione attuate e dei dispositivi di protezione individuali adottati, a seguito della valutazione di cui all'articolo 17, comma 1, lettera a);
c) il programma delle misure ritenute opportune per garantire il miglioramento nel tempo dei livelli di sicurezza;
d) l'individuazione delle procedure per l'attuazione delle misure da realizzare, nonché dei ruoli dell'organizzazione aziendale che vi debbono provvedere, a cui devono essere assegnati unicamente soggetti in possesso di adeguate competenze e poteri;
e) l'indicazione del nominativo del responsabile del servizio di prevenzione e protezione, del rappresentante dei lavoratori per la sicurezza o di quello territoriale e del medico competente che ha partecipato alla valutazione del rischio;
f) l'individuazione delle mansioni che eventualmente espongono i lavoratori a rischi specifici che richiedono una riconosciuta capacità professionale, specifica esperienza, adeguata formazione e addestramento.
3. Il contenuto del documento di cui al comma 2 deve altresì rispettare le indicazioni previste dalle specifiche norme sulla valutazione dei rischi contenute nei successivi titoli del presente decreto.
3.3.DECRETO LEGISLATIVO N° 81, 9 APRILE 2008, ARTICOLO 271 - VALUTAZIONE DEL RISCHIO
1. Il datore di lavoro, nella valutazione del rischio di cui all'articolo 17, comma 1, tiene conto di tutte le informazioni disponibili relative alle caratteristiche dell'agente biologico e delle modalità lavorative, ed in particolare:
a) della classificazione degli agenti biologici che presentano o possono presentare un pericolo per la salute umana quale risultante dall'allegato XLVI o, in assenza, di quella effettuata dal datore di lavoro stesso sulla base delle conoscenze disponibili e seguendo i criteri di cui all'articolo 268, commi 1 e 2;
b) dell'informazione sulle malattie che possono essere contratte;
c) dei potenziali effetti allergici e tossici;
d) della conoscenza di una patologia della quale è affetto un lavoratore, che è da porre in correlazione diretta all'attività lavorativa svolta;
e) delle eventuali ulteriori situazioni rese note dall'autorità sanitaria competente che possono influire sul rischio;
f) del sinergismo dei diversi gruppi di agenti biologici utilizzati.
2. Il datore di lavoro applica i principi di buona prassi microbiologica, ed adotta, in relazione ai rischi accertati, le misure protettive e preventive di cui al presente titolo, adattandole alle particolarità delle situazioni lavorative.
3. Il datore di lavoro effettua nuovamente la valutazione di cui al comma 1 in occasione di modifiche dell'attività lavorativa significative ai fini della sicurezza e della salute sul lavoro e, in ogni caso, trascorsi tre anni dall'ultima valutazione effettuata.
4. Nelle attività, quali quelle riportate a titolo esemplificativo nell'allegato XLIV, che, pur non comportando la deliberata intenzione di operare con agenti biologici, possono implicare il rischio di esposizioni dei lavoratori agli stessi, il datore di lavoro può prescindere dall'applicazione delle disposizioni di cui agli articoli 273, 274, commi 1 e 2, 275, comma 3, e 279, qualora i risultati della valutazione dimostrino che l'attuazione di tali misure non è necessaria.
5. Il documento di cui all'articolo 17 è integrato dai seguenti dati:
a) le fasi del procedimento lavorativo che comportano il rischio di esposizione ad agenti biologici;
b) il numero dei lavoratori addetti alle fasi di cui alla lettera a);
c) le generalità del responsabile del servizio di prevenzione e protezione dai rischi;
d) i metodi e le procedure lavorative adottate, nonché le misure preventive e protettive applicate;
e) il programma di emergenza per la protezione dei lavoratori contro i rischi di esposizione ad un agente biologico del gruppo 3 o del gruppo 4, nel caso di un difetto nel contenimento fisico.
6. Il rappresentante per la sicurezza è consultato prima dell'effettuazione della valutazione di cui al comma 1 ed ha accesso anche ai dati di cui al comma 5.
3.4.DECRETO LEGISLATIVO N° 81, 9 APRILE 2008, ARTICOLO 20 – OBBLIGHI DEI LAVORATORI
1. Ogni lavoratore deve prendersi cura della propria salute e sicurezza e di quella delle altre persone presenti sul luogo di lavoro, su cui ricadono gli effetti delle sue azioni o omissioni, conformemente alla sua formazione, alle istruzioni e ai mezzi forniti dal datore di lavoro.
2. I lavoratori devono in particolare:
a) contribuire, insieme al datore di lavoro, ai dirigenti e ai preposti, all'adempimento degli obblighi previsti a tutela della salute e sicurezza sui luoghi di lavoro;
b) osservare le disposizioni e le istruzioni impartite dal datore di lavoro, dai dirigenti e dai preposti, ai fini della protezione collettiva e individuale;
c) utilizzare correttamente le attrezzature di lavoro, le sostanze e le miscele pericolose, i mezzi di trasporto, nonché i dispositivi di sicurezza;
d) utilizzare in modo appropriato i dispositivi di protezione messi a loro disposizione;
e) segnalare immediatamente al datore di lavoro, al dirigente o al preposto le deficienze dei mezzi e dei dispositivi di cui alle lettere c) e d), nonché qualsiasi eventuale condizione di pericolo di cui vengano a conoscenza, adoperandosi direttamente, in caso di urgenza, nell'ambito delle proprie competenze e possibilità e fatto salvo l'obbligo di cui alla lettera f) per eliminare o ridurre le situazioni di pericolo grave e incombente, dandone notizia al rappresentante dei lavoratori per la sicurezza;
f) non rimuovere o modificare senza autorizzazione i dispositivi di sicurezza o di segnalazione o di controllo;
g) non compiere di propria iniziativa operazioni o manovre che non sono di loro competenza ovvero che possono compromettere la sicurezza propria o di altri lavoratori;
h) partecipare ai programmi di formazione e di addestramento organizzati dal datore di lavoro;
i) sottoporsi ai controlli sanitari previsti dal presente decreto legislativo o comunque disposti dal medico competente.
3. I lavoratori di aziende che svolgono attività in regime di appalto o subappalto, devono esporre apposita tessera di riconoscimento, corredata di fotografia, contenente le generalità del lavoratore e l'indicazione del datore di lavoro. Tale obbligo grava anche in capo ai lavoratori autonomi che esercitano direttamente la propria attività nel medesimo luogo di lavoro, i quali sono tenuti a provvedervi per proprio conto.
Nota a margine: l’articolo verte sugli obblighi di osservanza del lavoratore in merito alle procedure a tutela della sicurezza nei luoghi di lavoro e all’uso corretto dei mezzi di protezione individuale e collettiva (di carattere strutturale) e di controllo sanitario al fine di verificare uno stato di salute conforme e non pregiudicato dall’attività lavorativa (idoneità). Questo articolo quindi non va utilizzato per attribuire al lavoratore obblighi di osservanza di disposizioni sanitarie di profilassi come le vaccinazioni.
4.CONSIDERAZIONI GENERALI INERENTI ALLA MEDICINA DEL LAVORO
Un primo aspetto da sottolineare è che attualmente il lavoratore viene chiamato (attualmente) a vaccinarsi quale cittadino e non quale lavoratore, la vaccinazione è messa a disposizione dello Stato tramite il Servizio Sanitario Nazionale “in ordine di priorità, che tiene conto del rischio di malattia, dei tipi di vaccino e della loro disponibilità” (vedi Piano Strategico, Vaccinazione anti Sars-Cov-2/Covid19. Aggiornamento 12.12.2020).
In questo contesto l’unico compito che può avere il datore di lavoro (parliamo di attività sanitarie e sociosanitarie chiamate per prime alla vaccinazione) è quello di agevolare “domanda e offerta” ovvero inviare i nominativi dei propri operatori che corrispondono alle caratteristiche previste dalle norme con i soggetti pubblici che effettuano le vaccinazioni (USL/ASL/ATS/ASST).
La risposta, positiva o negativa che sia, del lavoratore è una questione coperta da privacy e riguarda il lavoratore con il soggetto sanitario corrispondente che sarà la struttura pubblica “vaccinante” o il medico competente se quest’ultima fa da tramite.
Sarà il medico competente, il cui ruolo come si vedrà è centrale in tutta questa materia per i poteri e di doveri che gli sono conferiti dal D.lgs. 81/2008, a valutare se la mancata adesione alla vaccinazione del cittadino può avere degli effetti sul lavoratore in funzione dei rischi della sua mansione.
Soprattutto occorre che i lavoratori siano ben coscienti che il giudizio di idoneità alla mansione che hanno ricevuto all’esito dell’ultima sorveglianza sanitaria fa testo fino a quando non viene sostituito da un altro, in altri termini un lavoratore può essere considerato (temporaneamente o meno) non idoneo alla mansione per un rischio “biologico” SOLO se tale condizione viene attestata dal medico competente con un nuovo giudizio di (non) idoneità sanitaria che andrà a sostituire l’ultimo.
Nota a margine: Come previsto dall’art. 41 del d.lgs. 81/2008 il lavoratore ha comunque diritto a ricorrere avverso il giudizio di idoneità o non idoneità sanitaria espressa dal medico competente entro 30 giorni (sono tassativi!) dalla ricezione del giudizio.
4.1.LE NOVITÀ NORMATIVE IN TERMINI DI LIVELLO DI RISCHIO DELL’AGENTE PATOGENO SARS-COV2
Occorre considerare una novità normativa introdotta con la direttiva UE 739 del 3.06.2020 che ha determinato il passaggio di classificazione del Sars-Cov2 da agente biologico lavorativo di categoria 2 a categoria 3 richiedendo la modifica degli allegati XLVII e XLVIII del dlgs 81/2008 (la direttiva era da recepire entro il 24.11.2020 ed è stata recepita con DL 149 del 9.11.2020 all’art. 17).
La classificazione nel livello di rischio 3 significa che l’agente biologico “può causare gravi malattie agli uomini e presenta una grave rischio per i lavoratori; può anche presentare un rischio di contagio nei confronti della comunità, ma in linea generale sono disponibili protocolli di profilassi e di trattamento ragionevolmente efficaci”. I virus SARS and MERS, ad esempio, appartengono alla categoria 3 (su una scala da 1, meno pericolosi, a 4 estremamente pericolosi).
A questo punto, come afferma giustamente anche Guariniello, risulta pacifico che il contesto della vaccinazione anticovid quale misura di protezione per esigenze lavorative si pone dentro la valutazione dei rischi da agenti biologici.
La premessa di tutto è quindi il riconoscimento che in quella data azienda/attività esiste un rischio lavorativo da agente biologico Sars-Cov2 (quindi di categoria 3).
Questa osservazione porta necessariamente a distinguere, nella successiva valutazione dei casi, tra attività già soggette a rischi da agenti biologici (come attività sanitarie e socio-sanitarie) e attività in precedenza non soggette a rischi da agenti biologici (o soggetti solo ad agenti di prima categoria).
Tali rischi sono principalmente connessi al settore sanitario, allevamento degli animali, gestione dei rifiuti e delle acque reflue, attività agricola e viaggi per lavoro.
Contrariamente a tale assunto l’Ispettorato Nazionale del Lavoro ha definito, nell’individuare le modalità di accesso nelle aziende per la verifica dei protocolli tra le parti sociali (14.03.2020 e 24.04.2020) che, per quanto riguarda il Covid19:
“Il rischio non è riconducibile al titolo X del Dlgs 81/2008, non attendendo ordinariamente al ciclo produttivo aziendale (Circolare INL, n. 149 del 20.04.2020)”.
Questa indicazione è, notoriamente, messa in discussione da diversi interpreti (tra cui il Dr. Guariniello) ma costituisce prassi che, dal livello ministeriale rappresentato dall’Ispettorato Nazionale del Lavoro, si è riverberata su tutti gli altri organi di vigilanza e principalmente sulle USL/ASL.
Nessuna azienda industriale, dei servizi e commerciale, ove l’unico rischio biologico è quello “esogeno” Covid-19, è stata infatti finora sanzionata per la assenza di un documento di valutazione dei rischi (DVR) dedicato a tale rischio ma si è proceduto alla verifica dell’attuazione corretta del protocollo tra le parti sociali4 comprese le eventuali violazioni su aspetti comunque previsti dal d.lgs. 81/2008 (come la pulizia dei locali, i dispositivi di protezione individuali, la formazione/informazione dei lavoratori ecc.).
Il protocollo è infatti stato inteso come il risultato di una valutazione dei rischi svolta dal Governo e valida per tutte le aziende/attività.
Un possibile “obbligo” vaccinale per mantenere la propria idoneità alla mansione potrebbe essere solo il risultato di un processo valutativo che porta il medico competente a definire come necessario “mettere a disposizione” dei lavoratori uno o più vaccini specifici. Quindi:
- se in una azienda non vi è un DVR che identifica il rischio biologico Covid come proprio della attività, e …
- non vi è sorveglianza sanitaria dedicata per il rischio biologico Covid, …
non si capisce da dove potrebbe sorgere un obbligo vaccinale lavorativo!
In caso contrario, infatti, le aziende sottoposte a vigilanza dal 5 maggio 2020 dovevano necessariamente garantire un DVR “Covid-correlato” e la assenza doveva attivare i “tradizionali” atti di contestazione, contravvenzione e prescrizione previsti dal D.lgs. 81/2008 e dal Dlgs 759/1994.
Quindi dobbiamo sempre distinguere tra:
- attività già in precedenza soggette a rischio biologico e quindi dotate di DVR dedicato e …
- quelle che “ex novo” hanno dovuto affrontare questo rischio.
4.2.ATTIVITÀ GIÀ SOGGETTE A RISCHIO BIOLOGICO (ES. ATTIVITÀ SANITARIE E SOCIO-SANITARIE)
In questo caso ci aspettiamo di trovarci di fronte a un pregresso DVR ove sono individuati i possibili agenti biologici determinati principalmente dal contatto/cura di e con utenti/pazienti e/o da attività di laboratorio su campioni biologici.
Il DVR dovrebbe contenere gli agenti individuati e la loro categoria in relazione alla mansione dei singoli lavoratori (ad es. reparti “infettivi” e non), definita una sorveglianza sanitaria specifica da parte del medico competente come pure la individuazione o meno della “opportunità” di effettuazione di vaccinazioni a partire da quelle che le norme individuano come obbligatorie.
In ogni caso, prima di parlare di “obblighi” dei lavoratori sulla base dell’art. 279 occorre verificare se il datore di lavoro ha adempiuto ai propri obblighi di valutazione ex art. 271 del d.lgs. 81/2008 (previa consultazione del RLS).
Dopodiché, all’esito della valutazione,
- il medico competente ha attivato la sorveglianza sanitaria e …
- definito la necessità/opportunità che ai lavoratori - non già immunizzati - propone il vaccino anticovid,
- In caso di rifiuto, il medico competente deve valutare se il lavoratore è ancora idoneo alla mansione cui è adibito,
- In caso contrario dovrà redigere e consegnare al lavoratore un giudizio di non idoneità (temporanea) alla mansione,
- nonché informare il datore di lavoro di questa nuova condizione del lavoratore affinché lo stesso sia adibito ad altra mansione (se esistente) cui la limitazione (non idoneità) non determina impedimenti al suo svolgimento.
Solo a questo punto può verificarsi la “occasione” del datore di lavoro per licenziare il lavoratore/lavoratrice ove non possa adibirlo ad altra mansione.
Un flusso ben definito con una serie di passaggi obbligati e “incatenati” tra loro a carico del datore di lavoro e del medico competente, in primis, e di converso del RSPP, come pure di diritti del RLS (e dei lavoratori/lavoratrici).
Riconoscere che l’attività sia soggetta a rischio biologico da Sars Cov 2 significa, come detto, individuare la presenza di un rischio da un agente di gruppo 3.
Questo riconoscimento determina a sua volta una serie di obblighi aggiuntivi (se l’attività non era già soggetta a un rischio per un altro agente del medesimo gruppo), in particolare (e non esaustivamente):
- Comunicazione alla ASL dell’esercizio di una attività che comporta l’uso di un agente biologico di tale gruppo (il che è palesemente in contrasto con la prassi che considera il Sars-Cov-2 un agente esogeno e non intenzionalmente prodotto).
- Attuare le misure tecniche, organizzative, procedurali (art. 272).
- Attuare le misure igieniche (art. 273)
- Definire misure di emergenza (art. 277)
- Fornire informazione e formazione ai lavoratori (art. 278)
- Registro nominativo degli esposti all’agente da inviare ad INAIL e tenere aggiornato (art. 280 d.lgs. 81/2008).
In altri termini, se si vuole “attivare” un obbligo vaccinale per motivi lavorativi con riferimento all’art. 279 del D.lgs. 81/2008 occorre rispettare anche gli articoli precedenti e successivi, le norme sulla sicurezza e l’igiene del lavoro non si applicano “a piacere”.
5.IL RISCHIO SPECIFICO IN AMBITO SANITARIO
In questo caso ci aspettiamo di trovarci di fronte a un pregresso DVR ove sono individuati i possibili agenti biologici determinati principalmente dal contatto/cura di e con utenti/pazienti e/o da attività di laboratorio su campioni biologici.
Il DVR dovrebbe contenere gli agenti individuati e la loro categoria in relazione alla mansione dei singoli lavoratori (ad es. reparti “infettivi” e non), definita una sorveglianza sanitaria specifica da parte del medico competente come pure la individuazione o meno della “opportunità” di effettuazione di vaccinazioni a partire da quelle che le norme individuano come obbligatorie.
In ogni caso, prima di parlare di “obblighi” dei lavoratori sulla base dell’art. 279 occorre verificare se il datore di lavoro ha adempiuto ai propri obblighi di valutazione ex art. 271 del d.lgs. 81/2008 (previa consultazione del RLS).
Dopodiché, all’esito della valutazione,
- il medico competente ha attivato la sorveglianza sanitaria e …
- definito la necessità/opportunità che ai lavoratori - non già immunizzati - propone il vaccino anticovid,
- In caso di rifiuto, il medico competente deve valutare se il lavoratore è ancora idoneo alla mansione cui è adibito,
- In caso contrario dovrà redigere e consegnare al lavoratore un giudizio di non idoneità (temporanea) alla mansione,
- nonché informare il datore di lavoro di questa nuova condizione del lavoratore affinché lo stesso sia adibito ad altra mansione (se esistente) cui la limitazione (non idoneità) non determina impedimenti al suo svolgimento.
Solo a questo punto può verificarsi la “occasione” del datore di lavoro per licenziare il lavoratore/lavoratrice ove non possa adibirlo ad altra mansione.
Un flusso ben definito con una serie di passaggi obbligati e “incatenati” tra loro a carico del datore di lavoro e del medico competente, in primis, e di converso del RSPP, come pure di diritti del RLS (e dei lavoratori/lavoratrici).
Riconoscere che l’attività sia soggetta a rischio biologico da Sars Cov 2 significa, come detto, individuare la presenza di un rischio da un agente di gruppo 3.
Questo riconoscimento determina a sua volta una serie di obblighi aggiuntivi (se l’attività non era già soggetta a un rischio per un altro agente del medesimo gruppo), in particolare (e non esaustivamente):
- Comunicazione alla ASL dell’esercizio di una attività che comporta l’uso di un agente biologico di tale gruppo (il che è palesemente in contrasto con la prassi che considera il Sars-Cov-2 un agente esogeno e non intenzionalmente prodotto).
- Attuare le misure tecniche, organizzative, procedurali (art. 272).
- Attuare le misure igieniche (art. 273)
- Definire misure di emergenza (art. 277)
- Fornire informazione e formazione ai lavoratori (art. 278)
- Registro nominativo degli esposti all’agente da inviare ad INAIL e tenere aggiornato (art. 280 d.lgs. 81/2008).
In altri termini, se si vuole “attivare” un obbligo vaccinale per motivi lavorativi con riferimento all’art. 279 del D.lgs. 81/2008 occorre rispettare anche gli articoli precedenti e successivi, le norme sulla sicurezza e l’igiene del lavoro non si applicano “a piacere”.
Come abbiamo visto dalla citazione delle principali norme che sottendono alla valutazione e alla gestione del rischio sanitario nei luoghi di lavoro, il legislatore intende focalizzare gli interventi nell’ambito specifico dell’attività (o delle attività) lavorativa svolta.
L’ambito sanitario non è esente da questa impostazione ma è ovviamente sensibile al rischio biologico, in misura molto maggiore degli altri ambienti di lavoro, in particolare nei reparti di malattie infettive. Tuttavia, va osservato che questa tipologia di rischio è costantemente presente per tutta una serie di agenti infettivi, al di là dell’attuale emergenza Covid-19, con ciò evidenziando che la Valutazione del Rischio in tali ambiti lavorativi deve essere coerente con l’impostazione caratteristica adottata anche in passato. L’emergenza Covid-19 non fa che incrementare il rischio biologico di una ulteriore “entità biologica”.
Di conseguenza sia le misure di protezione individuale che i protocolli sanitari collegati alle mansioni lavorative, definite nel DVR, devono essere coerenti con le impostazioni adottate finora: come conseguenza di questo, le misure di prevenzione e protezione devono seguire questa coerenza, sia in termini di adozione dei cosiddetti DPI (Dispositivi di Protezione Individuale) sia in termini di protocollo sanitario.
In primo luogo, quindi, i DVR in ambito ospedaliero o in ambienti affini come le RSA, case di cura ecc., devono essere stati aggiornati per la gestione del rischio da Covid-19 a partire dallo stato di emergenza sanitaria e dalla prima manifestazione della “pandemia” nel febbraio 2020.
Va quindi valutato se e in che misura la disponibilità di vaccini per Covid-19 sia necessaria per ridurre ulteriormente il rischio residuo di infezione e di diffusione dell’infezione nello specifico ambito lavorativo, soprattutto in relazione al rischio generalizzato di contrarre e diffondere l’infezione in generale.
In assenza di queste valutazioni, fatte alla luce delle informazioni sui profili di efficacia e sicurezza dei vaccini attualmente disponibili, non è possibile stabilire la necessità di una profilassi vaccinale specifica per Covid-19, senza contare che i profili di sicurezza a medio-lungo termine dei vaccini non sono ancora noti, profilandosi così l’eventualità di esporre i lavoratori ad altri rischi potenziali non noti (va sottolineato il fatto che i vaccini sono utilizzati in fase IV di sperimentazione e che i risultati definitivi saranno disponibili non prima del 2022/23).
A tale proposito entra a pieno titolo l’art. 279 del D.lgs 81/08 al comma 2:
- Il datore di lavoro, su conforme parere del medico competente, adotta misure protettive particolari per quei lavoratori per i quali, anche per motivi sanitari individuali, si richiedono misure speciali di protezione, fra le quali:
a) la messa a disposizione di vaccini efficaci per quei lavoratori che non sono già immuni all'agente biologico presente nella lavorazione, da somministrare a cura del medico competente;
Quindi:
- Le misure vanno adottate in genere per un gruppo limitato di lavoratori a cui vanno indirizzate “misure speciali” (e non generalizzate) di protezione, funzionali allo svolgimento della mansione specifica;
- Possono essere considerate motivazioni sanitarie individuali;
- Vanno messi a disposizione vaccini efficaci;
- Vanno considerate le condizioni di immunità dei lavoratori all’agente biologico;
Relativamente a questo ultimo punto, Per espressa indicazione di AIFA, coloro che hanno avuto una diagnosi di positività a COVID-19 non necessitano di una vaccinazione nella prima fase della campagna vaccinale, mentre potrebbe essere considerata quando si otterranno dati sulla durata della protezione immunitaria.5
In conclusione, il lavoratore in ambito sanitario dovrà rapportarsi al proprio dirigente mettendo in evidenza gli argomenti su esposti, senza assumere una posizione di rifiuto della profilassi a prescindere. Fatte le necessarie verifiche documentali (DVR), secondo le procedure canoniche (coinvolgimento RLS, come esposto in precedenza) il lavoratore potrà assumere una posizione consapevole e INFORMATA, esprimendo in tal modo un consenso o un dissenso adeguato.
La produzione normativa viene descritta sinteticamente nella pagina del ministero dedicata agli operatori sanitari6.
Il documento che fornisce elementi generali per rafforzare la preparedness e fronteggiare in modo ottimale le nuove infezioni da SARS-CoV-2 nella stagione autunno-inverno 2020-2021 alla luce di tutti i possibili scenari epidemici che dovessero delinearsi è definito “Prevenzione e risposta a COVID-19: evoluzione della strategia e pianificazione nella fase di transizione per il periodo autunno-invernale”7.
Il Parlamento ha approvato il 2 dicembre 2020 le linee guida del Piano strategico per la vaccinazione anti-SARS-CoV-2/COVID-19: il piano e le circolari attuative sono disponibili in rete8.
Quello che va messo in luce in questo caso è il carattere generale del piano, aspecifico per il settore sanitario, quindi non determina alcunché in merito ad eventuali disposizioni in materia di vaccinazioni per Covid-19 (quantunque un piano non potrebbe in ogni caso determinare obblighi in tal senso).
Tale piano si esprime attraverso il Decreto del Ministro della salute 2 gennaio 20219.
In merito alla protezione degli operatori sanitari le linee guida sono espresse nel “Rapporto ISS COVID-19 n. 2/2020 - aggiornato al 28 marzo 2020”10.
Va sottolineato, in conclusione che, al momento, non esiste una produzione normativa specifica per gli operatori sanitari in termini di obblighi vaccinali per Covid-19.
Per ogni ulteriore approfondimento istituzionale vi invitiamo a consultare le pagine ministeriali all’indirizzo http://www.salute.gov.it/portale/nuovocoronavirus/dettaglioContenutiNuovoCoronavirus.jsp?lingua=italiano&id=5383&area=nuovoCoronavirus&menu=vuoto#:~:text=In%20accordo%20con%20il%20Governo,stato%20integrato%20il%2024%20aprile.
Va sottolineato che le indicazioni tuttora presenti in queste pagine sono (citiamo):
Le più efficaci misure di prevenzione da applicare sia nell’ambito comunitario che sanitario, includono:
- praticare frequentemente l’igiene delle mani con acqua e sapone o, se questi non sono disponibili, con soluzioni/gel a base alcolica. In ambito sanitario è raccomandato l’uso preferenziale di soluzioni/gel a base alcolica, in modo da consentire l’igiene delle mani al letto del paziente in tutti i momenti raccomandati (prima e dopo il contatto, prima di manovre asettiche, dopo il contatto con liquidi biologici, dopo il contatto con le superfici in vicinanza del paziente);
- evitare di toccare gli occhi, il naso e la bocca con le mani;
- tossire o starnutire all’interno del gomito con il braccio piegato o di un fazzoletto, preferibilmente monouso, che poi deve essere immediatamente eliminato;
- indossare la mascherina chirurgica nel caso in cui si abbiano sintomi respiratori ed eseguire l’igiene delle mani dopo avere rimosso ed eliminato la mascherina;
- evitare contatti ravvicinati mantenendo la distanza di almeno un metro dalle altre persone, in particolare con quelle con sintomi respiratori.
Precauzioni aggiuntive sono necessarie per gli operatori sanitari al fine di preservare sé stessi e prevenire la trasmissione del virus in ambito sanitario e sociosanitario. Tali precauzioni includono l’utilizzo corretto dei DPI e adeguata sensibilizzazione e addestramento alle modalità relative al loro uso, alla vestizione, svestizione ed eliminazione, tenendo presente che alla luce delle attuali conoscenze, le principali modalità di trasmissione del SARS-CoV-2 sono attraverso droplet e per contatto, a eccezione di specifiche manovre e procedure a rischio di generare aerosol (Allegato 1). È quindi sempre particolarmente importante praticare l’igiene delle mani per prevenire la trasmissione da contatto, soprattutto in relazione con l’utilizzo corretto dei DPI.
6.INFORMAZIONI SUL FARMACO
6.1.DIRITTO ALL’INFORMAZIONE
In ambito sanitario, quello di nostro specifico interesse, il progresso delle conoscenze scientifiche e dei mezzi tecnologici ha aperto nuove problematiche sul piano etico, ponendo le persone di fronte a scelte spesso molto complesse, per assumere le quali risulta fondamentale la corretta informazione da parte del professionista, anche per gli obblighi deontologici connessi.
Il Consenso Informato (CI) rappresenta certamente un momento particolare, ponendosi come strumento che contribuisce allo stabilirsi dell’alleanza terapeutica.
Consenso deve significare partecipazione, consapevolezza, informazione11, libertà di scelta e di decisione delle persone. Il consenso informato HA le seguenti caratteristiche principali:
- Deve essere esplicitamente manifestato mediante un comportamento che riveli in maniera precisa e inequivocabile il proposito di sottoporsi a quello specifico trattamento sanitario. Ciò significa che l’interessato deve dimostrare di avere ben capito il motivo, gli effetti e le possibili alternative del trattamento al quale sta per sottoporsi;
- Può essere prestato solo dall’interessato (ad eccezione dei minorenni o delle persone sottoposte a tutela);
- Deve essere libero, nel senso che deve essere il frutto di un convincimento personale dell’interessato che ha già ricevuto le informazioni necessarie;
- L’informazione fornita deve essere la più completa possibile, … nonché di tutti gli eventuali interventi o terapie alternative;
- Può essere revocato anche poco prima che l’intervento inizi;
Altre caratteristiche importanti sono:
- La persona deve essere sempre informata su tutte le alternative terapeutiche (…);
- La persona deve essere informata dell’esperienza e della casistica dell’operatore e/o dell’unità operativa in merito all’intervento a cui si dovrà sottoporre.
Fatte queste premesse vediamo per punti le questioni rilevanti che presiedono all’eventuale adesione verso la somministrazione di Comirnaty.
6.2.COMIRNATY È UN VACCINO?
Secondo la definizione di AIFA12, pacificamente e ampiamente riconosciuta, i vaccini sono medicinali biologici, infatti, le “sostanze attive” dei vaccini sono rappresentate da: microrganismi (batteri o virus) opportunamente inattivati o uccisi in maniera tale da stimolare il sistema immunitario senza causare la malattia; parti specifiche (antigeni) dei microrganismi che sono coinvolte direttamente nella risposta del sistema immunitario a quel patogeno; sostanze prodotte dal microrganismo stesso (tossine) e coinvolte nel meccanismo con cui quel patogeno determina la malattia, rese sicure ed efficaci attraverso il processo di produzione del vaccino.
Il principio attivo di Comirnaty è rappresentato da RNA messaggero (mRNA), prodotto mediante trascrizione in vitro senza l’ausilio di cellule (cell-free) dai corrispondenti DNA stampo13, ossia una molecola sintetica che mima l’RNA virale al fine di ottenere un’azione sulle nostre cellule; in Comirnaty non vi è virus, né sue parti, neppure depotenziate o inattivate.
Comirnaty, pertanto, sembra non possedere alcuna caratteristica che denota un vaccino.
L’azienda Moderna che ha sviluppato un farmaco contro la covid-19 basato sempre su mRNA paragona l’mRNA a un software, una “app”, affermando, altresì, di aver creato una piattaforma tecnologica mRNA che funziona in modo molto simile a un sistema operativo su un computer14.
6.3.COPERTURA IMMUNITARIA ED EFFICACIA DI COMIRNATY
Oggi non è nota la durata della immunità15 e non è nota la capacità del trattamento di fermare l’infezione16.
Numerosi fatti di cronaca riferiscono di focolai Covid in ospedali e soprattutto in case di cura e RSA17 a distanza di pochi giorni dalla somministrazione della prima dose di Comirnaty, anche in contesti in cui non si registravano in precedenza casi Covid positivi. Circostanze simili si stanno registrando anche fra coloro che hanno completato il trattamento con la seconda dose.18
Sebbene si legga sul RCP che i soggetti potrebbero non essere completamente protetti fino a 7 giorni dopo la seconda dose del “vaccino”, questi focolai, non circoscritti all’Italia, appaiono piuttosto anomali.
Negli USA Il programma di prevenzione della Covid-19 coincide con un'impennata dei decessi legati al COVID-19 nelle case di cura e nelle strutture di assistenza per adulti di New York19.
Osservando le segnalazioni spontanee di reazioni avverse registrate nella banca dati europea delle segnalazioni di sospette reazioni avverse ai farmaci, EudraVigilance20, si registrano al 6 febbraio 402 casi di positività a Sars Cov-2 (spesso segnalate come “drug ineffective”), di cui 16 con esito fatale. I casi di positività a Sars Cov-2 definiti GRAVI rappresentano il 5,85% del totale delle segnalazioni ADR gravi (209 su 5109).
Peter Doshi, uno dei massimi esperti a livello mondiale di trial clinici, riguardo all'efficacia del trattamento Comirnaty, insiste nell’affermare che “abbiamo bisogno di maggiori dettagli e dati grezzi” per poter affermare che il “vaccino” Pfizer-BioNTech sia veramente efficace, almeno nella misura dichiarata dal produttore21.
6.4.QUESITI APERTI
|
SULLE TERAPIE GENICHE |
È possibile affermare che il trattamento sanitario proposto sia di fatto una terapia genica? Chiarire questa circostanza assume particolare importanza in termini di valutazione di possibili alternative terapeutiche. |
|
SU EFFICACIA E SICUREZZA DELLA PROFILASSI PROPOSTA |
E’ stata valutata la copertura immunitaria attesa, unitamente alle misure di controllo dell’efficacia vaccinale? In mancanza di una ragionevole certezza riguardo alla copertura immunitaria (efficacia) presunta quali sono le ulteriori misure previste dal DVR e dal protocollo sanitario aziendale? |
|
SUL DVR |
Quali sono le misure previste dal DVR e dal protocollo sanitario aziendale al fine di prevenire gli eventuali focolai da Covid-19 che potrebbero ipoteticamente verificarsi – come suggeriscono le note di cronaca disponibili – a fronte della campagna vaccinale prevista? |
7.RISCHI COLLEGATI ALLA PROPOSTA DI SOMMINISTRAZIONE DI COMIRNATY
7.1.RISCHI COLLEGATI ALLA AUTORIZZAZIONE ALL'IMMISSIONE IN COMMERCIO CONDIZIONATA (CMA, CONDITIONAL MARKETING APPROVAL)
Comirnaty è utilizzato in Italia attraverso la procedura di autorizzazione all'immissione in commercio condizionata (CMA, Conditional Marketing Approval)22, concepita per consentire l'autorizzazione all'immissione in commercio il più rapidamente possibile, non appena disponibili dati sufficienti presentati dallo sviluppatore del “vaccino” nel corso delle "revisioni a rotazione”23.
Per il farmaco anti-Covid Comirnaty l’autorizzazione condizionata sarà in futuro convertita in STANDARD MARKETING AUTHORIZATION?
È possibile che non si possa rispondere a questa domanda.
Si legge, infatti, nel Rapporto pubblico di valutazione (EPAR public Assessment report) del farmaco Comirnaty di Pfizer-BioNTech24:
“È probabile che il richiedente sarà in grado di fornire dati completi. Il Richiedente intende continuare lo studio di Fase 3 in corso con i partecipanti come originariamente assegnato il più a lungo possibile, per ottenere dati a lungo termine e per garantire un seguito sufficiente a sostegno di un'autorizzazione all'immissione in commercio standard. In caso di disponibilità di un qualsiasi vaccino COVID-19.
Lo sponsor farà appello ai partecipanti affinché rimangano nello studio in corso come originariamente randomizzato il più a lungo possibile, idealmente fino a quando un vaccino COVID-19 avrà la piena approvazione regolamentare.
In tutti i casi, si intende seguire i partecipanti fino ai 24 mesi previsti originariamente dopo la vaccinazione, indipendentemente dal fatto che i partecipanti scelgano di passare dal placebo alla vaccinazione attiva.”
È CHIARO CHE LA FUORIUSCITA DEI PARTECIPANTI DALLO STUDIO CARDINE, QUELLO SU CUI SI È BASATA L’AUTORIZZAZIONE ALL’IMMISSIONE IN COMMERCIO CONDIZIONATA, INFICEREBBE LA POSSIBILITÀ DI COMPLETARE/INTEGRARE GLI STUDI E DI CONFERMARE I BENEFICI DEL VACCINO; INFATTI, “L’OBIETTIVO DELLO STUDIO È QUELLO DI VALUTARE LA SICUREZZA, LA TOLLERABILITÀ, L'IMMUNOGENICITÀ E L'EFFICACIA DEL VACCINO M-RNA COVID-19.”
L’eventuale conferma, in ogni caso, potrebbe arrivare tra due anni.
Il titolare della licenza, infatti, dovrà presentare la relazione finale dello studio cardine, soggetta a Obbligo Specifico nel contesto di un'autorizzazione all'immissione in commercio condizionata, entro dicembre 2023.
Direttamente dalla voce di una volontaria allo studio, intervistata dalla redazione della trasmissione televisiva Report andata in onda lo scorso 25 gennaio su RAI 325, si è appreso che al gruppo placebo è offerta la somministrazione di Comirnaty:
“Ora che lo studio è completo io voglio il vaccino, mi faranno altri esami e se ero nel gruppo placebo mi daranno subito il vaccino perché i volontari possono saltare la coda”.
Negli USA, invece, si è optato per un'autorizzazione all'uso d'emergenza (EUA)26 che consente l'uso temporaneo del vaccino, che rimane tuttavia privo di licenza, ossia non approvato e non immesso in commercio, contrariamente a quanto previsto da un'autorizzazione all'immissione in commercio (condizionata).
"In una situazione di autorizzazione d’emergenza (EUA) per l’utilizzo di un vaccino, per quanto sia possibile date le circostanze, la FDA deve garantire che i destinatari di tale vaccino (autorizzato per l’uso in emergenza) siano accuratamente informati del fatto che il farmaco è soggetto a questo tipo di autorizzazione, dei benefici e dei rischi noti e potenziali, della misura in cui tali benefici e rischi sono sconosciuti, del fatto che sia possibile accettare o rifiutare il vaccino, e di qualsiasi alternativa disponibile al prodotto.”
Il Financial Times27 è venuto a conoscenza di un promemoria diffuso ai membri da Vaccines Europe, una divisione della Federazione Europea delle Industrie e delle Associazioni Farmaceutiche (European Federation of Pharmaceutical Industries and Associations, EFPIA) e ne riporta uno stralcio:
"La velocità e la portata dello sviluppo e del lancio impediscono di produrre la stessa quantità di evidenze fondamentali che normalmente sarebbero disponibili attraverso studi clinici estesi nel tempo e attraverso l’esperienza degli operatori sanitari”.
Nel documento si afferma che ciò crea rischi “inevitabili” e che va sostenuto un
"sistema di indennizzo totalmente privo di responsabilità e di contraddittorio oltre all'esenzione da responsabilità civile”28.
Recentemente la Commissione Europea ha messo a disposizione, in un primo momento solo agli europarlamentari (in una stanza con l’impossibilità di prendere appunti o scattare fotografie), poi ai cittadini con la pubblicazione sul sito, l’Accordo di Acquisto Preliminare (Advance Purchase Agreement, APA) stipulato con l’azienda farmaceutica tedesca CureVac29 che ha previamente accettato di renderlo consultabile.
Anche se di fatto numerosissime parti risultano oscurate, in particolare quelle riferibili alla responsabilità dell’azienda in caso di danni dovuti al vaccino, alla voce “1.14. WARRANTIES; ACCEPTANCE MECHANISM” si può leggere:
“1.14.3. Dato lo stato attuale del programma di sviluppo clinico e alla luce delle circostanze straordinarie dell'esecuzione e delle prestazioni del presente APA, il contraente, in particolare, non garantisce che il Prodotto sarà sufficientemente efficace nella prevenzione dell'infezione della COVID-19 e/o possa manifestare eventi avversi inaccettabili oltre a quanto sarà successivamente documentato negli studi clinici in corso e in quelli pianificati o indicato nel foglietto illustrativo del Prodotto.”30
7.2.RISCHI COLLEGATI ALL’IMPIEGO DELLA TECNOLOGIA mRNA
Nella banca dati europea delle segnalazioni di sospette reazioni avverse31 al 21 gennaio sono registrati 245 decessi in Europa segnalati come eventi avversi dopo la somministrazione di Comirnaty (di cui 179 decessi sono avvenuti nei Paesi dell’Area Economica Europea, EEA)32.
Osservando i dati delle segnalazioni spontanee di reazioni avverse riportati fino al 5 febbraio nella banca dati EudraVigilance, nei paesi EEA si registra un notevole incremento dei casi con esito fatale: 508 decessi. I casi con esito fatale rappresentano il 9,94% delle segnalazioni ADR (Adverse Drug Reaction) classificate gravi e l’1,5% del totale delle segnalazioni.
Si tratta di segnalazioni spontanee e fra queste certamente non risulta il caso fatale della dott.ssa Gabriela Godoy33, farmacista e madre di quattro figli, sentitasi male il giorno dopo aver effettuato il Comirnaty e morta dopo 5 giorni di ospedalizzazione. Si apprende che si è trattato di un ictus, nessun esame autoptico, piuttosto i suoi organi sono stati espiantati per la donazione e la somministrazione di Comirnaty, un trattamento OGM sviluppato in pochi mesi con la tecnologia mRNA, fino a oggi mai stata oggetto di licenza da parte delle Autorità regolatorie e pertanto mai testata in condizioni reali e su vasta scala, rappresenta solo una triste coincidenza.
La tecnologia mRNA trae origine per la cura dei tumori e non è mai stata impiegata in clinica se non con qualche eccezione con scarsi risultati in termini di efficacia e con problematiche di sicurezza.34
Sulla base dei dati delle segnalazioni spontanee di reazioni avverse riportati fino al 5 febbraio (incluso) nella banca dati EudraVigilance, nei paesi EEA si registrano un totale di 33.925 casi, di cui 5.109 classificati come gravi (15,06%) e 28.816 classificati come non gravi (84,94%).
L'Italia risulta in assoluto il Paese con le maggiori segnalazioni: 14.673 (ovvero circa il 43%). Dal 2 al 5 febbraio sono state riportate in media 2.587 segnalazioni al giorno provenienti dai Paesi EEA. Se l'Italia seguisse questo trend, più di 1.000 segnalazioni al giorno potrebbero provenire dal nostro Paese.
7.3.RISCHIO COLLEGATO A UNA PRECEDENTE DIAGNOSI DI POSITIVITà A COVID-19
Per espressa indicazione di AIFA, “coloro che hanno avuto una diagnosi di positività a COVID-19 non necessitano di una vaccinazione nella prima fase della campagna vaccinale, mentre potrebbe essere considerata quando si otterranno dati sulla durata della protezione immunitaria35.”
Va rilevato, inoltre, che il profilo di sicurezza non è noto per gli individui con una precedente positività al COVID-19, in quanto tali soggetti sono stati esclusi dai trial clinici36.
7.4.RISCHI IDENTIFICATI, RISCHI POTENZIALI E INFORMAZIONI MANCANTI
È fondamentale che il medico competente, nel rispetto della privacy, sia messo al corrente di specifiche circostanze che per il principio di precauzione potrebbero rappresentare una controindicazione alla somministrazione del farmaco.
Lo sono a maggior ragione se si rientra nella casistica “rischi identificati” e “informazioni mancanti” riportati nel Riassunto delle Caratteristiche di Prodotto (RCP)37 e/o nel Risk Management Plan (RMP)38 pubblicati da EMA.
"IMPORTANTI RISCHI IDENTIFICATI: ANAFILASSI"
-
RISCHIO ANAFILASSI PER IPERSENSIBILITÀ AL PRINCIPIO ATTIVO O AD UNO QUALSIASI DEGLI ECCIPIENTI CONTENUTI NEL VACCINO
Nel Riassunto delle Caratteristiche di Prodotto si legge che l’ipersensibilità al principio attivo o ad uno qualsiasi degli eccipienti contenuti nel vaccino rappresenta una controindicazione alla vaccinazione.
Nel piano per la gestione del rischio (RMP) viene evidenziato come un importante rischio identificato.
Nell'European Public Assessment Report (EPAR)39 si evidenzia che nel prodotto finito sono inclusi due nuovi (mai utilizzati in vaccini iniettabili) eccipienti: il lipide cationico ALC-0315 e il lipide PEGilato ALC-0159 dei quali sono fornite informazioni limitate, ma allo sviluppatore non sono richiesti studi mirati riguardo alla sicurezza.
Si legge nel Rapporto pubblico di valutazione (EPAR Public Assessment Report):
“Questa preoccupazione per la sicurezza sarà seguita attraverso le attività di farmacovigilanza di routine e negli studi di sicurezza pianificati e in corso e sarà riportata nei rapporti mensili di sintesi sulla sicurezza e nei PSUR (Periodic Safety Update Reports).”
Alcuni esperti sospettano che le nanoparticelle lipidiche (LNP) che permettono al materiale genetico di penetrare all’interno delle cellule, essendo PEGilate – ovvero legate a un composto, il polietilenglicole (PEG) – possano indurre reazioni anafilattiche in individui con anticorpi PEG preesistenti. Janos Szebeni ha osservato un fenomeno causato da queste particelle che ha definito “complement activation–related pseudoallergy” (CARPA). Un gruppo di ricerca che nel 2014 aveva dovuto interrompere uno studio di fase III dopo che lo 0,6% circa delle 1600 persone che partecipavano allo studio aveva avuto reazioni anafilattiche. Il gruppo ha scoperto che ognuno di quelli che avevano avuto una anafilassi aveva un alto livello di IgG anti PEG e che altri che pure avevano IgG anti PEG elevate non avevano tuttavia reagito allo stesso modo.
Uno studio ungherese sugli anticorpi anti PEG rileva come “[..] le IgG e le IgM anti-PEG hanno dimostrato di essere responsabili della perdita di efficacia dovuta all'accelerazione della clearance del farmaco nel sangue (ABC) e delle reazioni di ipersensibilità (HSR) che comportano gravi sintomi allergici con anafilassi occasionalmente fatale.”40 Le risposte immunitarie specifiche verso queste sostanze, quindi, potrebbero ridurre l'efficacia dei vaccini41. Il fenomeno rimane oggetto di approfondimento.
Osservando i dati sulle segnalazioni spontanee di reazioni avverse registrate nella banca dati europea delle segnalazioni di sospette reazioni avverse ai farmaci, EudraVigilance42, si registrano al 6 febbraio 253 casi di anafilassi (di cui 216 segnalati come gravi e 37 come non gravi) e 376 casi di ipersensibilità (di cui 187 segnalati come gravi e 189 come non gravi) per un totale di 403 reazioni allergiche GRAVI di cui 2 segnalazioni con esito fatale, ovvero il 7,89% delle segnalazioni ADR definite GRAVI (403 su 5.109 segnalazioni classificate gravi).
-
RISCHIO ANAFILASSI PER GRAVE REAZIONE ALLERGICA A UN VACCINO
Nel Regno Unito nel “Package leaflet”43 viene indicato di confrontarsi con il proprio medico, farmacista o personale infermieristico nel caso in cui si avesse avuto in precedenza una grave reazione allergica a un vaccino, a un medicinale o anche a un alimento.
In un recente articolo, la rivista Science44 rileva che Pfizer nei trial clinici avrebbe escluso partecipanti che avevano avuto una reazione grave ad altri vaccini. Il profilo di sicurezza di Comirnaty per tali individui, pertanto, non è noto a causa della loro esclusione dallo studio clinico fondamentale.45
- RISCHIO ANAFILASSI PER GRAVE REAZIONE ALLERGICA A UN FARMACO O ANCHE A UN ALIMENTO O ANCHE A PUNTURE DI INSETTO
Dalle evidenze, il rischio che Comirnaty possa innescare anafilassi o gravi reazioni allergiche appare ben oltre la soglia osservata per altri vaccini. Tra gli individui che hanno subito la grave reazione avversa vi sono soggetti con una storia di allergie o reazioni allergiche a farmaci, cibi o punture di insetto46.
Nel Regno Unito nel “Package leaflet”47 viene indicato di confrontarsi con il proprio medico, farmacista o personale infermieristico nel caso in cui si avesse avuto in precedenza una grave reazione allergica a un vaccino, a un medicinale o anche a un alimento.
"IMPORTANTI RISCHI POTENZIALI: VACCINE-ASSOCIATED ENHANCED DISEASE (VAED), INCLUSA LA VACCINE-ASSOCIATED ENHANCED RESPIRATORY DISEASE (VAERD)”
NB: Questa indicazione NON è riportata nel Riassunto delle Caratteristiche di Prodotto (RCP)
Le malattie potenziate associate al vaccino (VAED) si verificano quando manifestazioni di infezioni cliniche modificate e/o più gravi colpiscono gli individui, precedentemente vaccinati, esposti all’infezione naturale (agente patogeno di tipo selvaggio) per lo stesso agente patogeno.
Il Piano per la gestione del rischio (RMP) del trattamento Comirnaty segnala un importante rischio potenziale che non è riportato né nel Riassunto delle Caratteristiche di Prodotto né tantomeno nel modulo di Consenso Informato: il rischio di Vaccine-Associated Enhanced Disease (VAED), inclusa la Vaccine-Associated Enhanced Respiratory Disease (VAERD)”.48
Si ipotizza che il rischio di incorrere in un tal fenomeno sia più alto negli individui che producono titoli anticorpali neutralizzanti inferiori o in quelli che dimostrano di perdere l’immunità.
Nulla è dato a sapere riguardo alle titolazioni anticorpali dei partecipanti allo studio cardine, né tantomeno se e in quale misura dimostrino di perdere l’immunità a seguito della somministrazione del farmaco.
Sulla base delle conoscenze su altri tipi di coronavirus, si stima che l’immunità sviluppata a seguito del trattamento potrebbe perdurare per 9-12 mesi49.
Si apprende dallo studio “Informed consent disclosure to vaccine trial subjects of risk of COVID‐19 vaccines worsening clinical disease”50 che il rischio di incorrere nel potenziamento della malattia non è né teorico, né inconfutabile.
“Il potenziamento della malattia indotto dal vaccino è stato osservato anche con i virus della SARS e della MERS e con il coronavirus felino, che sono strettamente correlati al SARS-CoV-2”.
RISCHI COLLEGATI ALLA MANCANZA DI DATI SULLA SICUREZZA PER L’USO IN GRAVIDANZA E DURANTE L’ALLATTAMENTO
Nel Riassunto delle Caratteristiche di Prodotto (RCP) troviamo le seguenti indicazioni:
“4.6 Fertilità, gravidanza e allattamento
Gravidanza
I dati relativi all’uso di Comirnaty in donne in gravidanza sono in numero limitato. Gli studi sugli animali non indicano effetti dannosi diretti o indiretti su gravidanza, sviluppo embrionale/fetale, parto o sviluppo post-natale (vedere paragrafo 5.3). La somministrazione di Comirnaty durante la gravidanza deve essere presa in considerazione solo se i potenziali benefici sono superiori ai potenziali rischi per la madre e per il feto.
Allattamento
Non è noto se Comirnaty sia escreto nel latte materno.”
Nel Piano per la gestione del rischio (RMP) si legge:
“Il profilo di sicurezza del vaccino non è noto nelle donne in gravidanza o in allattamento a causa della loro esclusione dallo studio clinico cardine.
Ci possono essere donne in gravidanza che scelgono di essere vaccinate nonostante la mancanza di dati sulla sicurezza. Sarà importante seguirle per gli esiti della gravidanza e del parto. I tempi della vaccinazione in una donna in gravidanza e la conseguente risposta immunitaria possono avere impatti variabili favorevoli o sfavorevoli sull’embrione/feto.”
RISCHI COLLEGATI ALLA MANCANZA DI DATI SULLA SICUREZZA PER L’USO IN SOGGETTI IMMUNOCOMPROMESSI
Nel Riassunto delle Caratteristiche di Prodotto (RCP) vengono fornite le seguenti indicazioni:
“Soggetti immunocompromessi
L’efficacia, la sicurezza e l’immunogenicità del vaccino non sono state valutate nei soggetti immunocompromessi, compresi quelli in terapia immunosoppressiva. L’efficacia di Comirnaty potrebbe essere inferiore nei soggetti immunocompromessi.”
Nel Piano per la gestione del rischio (RMP) si legge:
“Il profilo di sicurezza del vaccino non è noto negli individui immunocompromessi a causa della loro esclusione dallo studio clinico fondamentale. L'efficacia del farmaco può essere inferiore negli individui immunocompromessi, diminuendo così la loro protezione da COVID-19.”
RISCHI COLLEGATI ALLA MANCANZA DI DATI SULLA SICUREZZA PER L’USO IN PAZIENTI FRAGILI CON COMORBILITÀ (ad esempio, broncopneumopatia cronica ostruttiva – BPCO - diabete, malattie neurologiche croniche, disturbi cardiovascolari)
Nel Riassunto delle Caratteristiche di Prodotto troviamo le seguenti indicazioni:
“5.1 Proprietà farmacodinamiche
Non sono state rilevate differenze cliniche significative in termini di efficacia complessiva del vaccino nei partecipanti a rischio di COVID-19 severa, compresi quelli con uno o più̀ comorbilità suscettibili di aumentare il rischio di COVID-19 severa (ad es. asma, indice di massa corporea (IMC) ≥30 kg/m2, malattia polmonare cronica, diabete mellito, ipertensione).
(…)
Inoltre, le analisi per sottogruppi dell’endpoint primario di efficacia hanno dimostrato stime puntuali di efficacia paragonabili fra sessi, gruppi razziali ed etnie, e fra partecipanti con comorbilità associate a un rischio elevato di COVID-19 severa.”
Nel Piano per la gestione del rischio (RMP) si legge:
“Ci sono informazioni limitate sulla sicurezza del vaccino in pazienti fragili con comorbilità che sono potenzialmente a più alto rischio di COVID-19 grave.”
Comirnaty, si legge,
“è stato studiato in individui con malattie croniche stabili (ad esempio ipertensione, obesità), tuttavia non è stato studiato in individui fragili con gravi comorbilità che possono compromettere la funzione immunitaria”.
E nel seguito:
“I dati di sicurezza saranno raccolti in individui fragili a causa dell'età o di malattie debilitanti negli studi di sorveglianza attiva e attraverso la farmacovigilanza di routine.”
RISCHI COLLEGATI ALLA MANCANZA DI DATI SULLA SICUREZZA PER L’USO IN PAZIENTI CON DISTURBI AUTOIMMUNI O INFIAMMATORI
Nel Piano per la gestione del rischio (RMP) si legge:
“Ci sono informazioni limitate sulla sicurezza del vaccino in individui con disturbi autoimmuni o infiammatori e una preoccupazione teorica che il vaccino possa esacerbare la loro malattia di base.”
Questa indicazione NON è riportata nel Riassunto delle Caratteristiche di Prodotto (RCP).
E nel seguito:
“I dati sulla sicurezza saranno raccolti in individui con malattie autoimmuni o infiammatorie croniche, compresi quelli che potrebbero essere sotto immunosoppressori negli studi di sorveglianza attiva.”
RISCHI COLLEGATI ALLA MANCANZA DI DATI SULLA SICUREZZA A LUNGO TERMINE DEI FARMACI PRODOTTI CON TECNOLOGIA mRNA
Nel Piano per la gestione del rischio (RMP) di Comirnaty si legge:
“La sicurezza a lungo termine del vaccino m-RNA BNT162b2 è attualmente sconosciuta, tuttavia ulteriori dati sulla sicurezza sono in corso di raccolta nello studio C4591001 per un massimo di 2 anni dopo la somministrazione della seconda dose del vaccino m-RNA BNT162b2.”
Come anzidetto, la probabile fuoriuscita dei partecipanti dallo studio cardine, potrebbe inficiare la possibilità di completare/integrare gli studi e di confermare, pertanto, i benefici del vaccino.
Si apprende dalla stampa51 che Pfizer ha stretto un accordo con il ministero della Sanità israeliano, il quale garantisce “di fornire tutti i risultati delle vaccinazioni, compresi i dettagli di ogni singola puntura fino al braccio di inoculazione” come riporta il Corriere della Sera. Nell’articolo si legge anche che “Un’intesa simile sarebbe stata finalizzata anche con Moderna” trasformando Israele “in un laboratorio su scala nazionale”. L’accordo recentemente è stato reso pubblico52 ma oscurato per quel che riguarda la responsabilità della casa farmaceutica per gli effetti avversi al trattamento.
Nella “Scheda Informativa per gli operatori sanitari che somministrano il vaccino” Pfizer- BioNTech53, negli USA, la Food and Drug Administration (FDA) statunitense ha rilasciato un’Emergency Use Authorization (EUA) per consentire l'uso d'emergenza del prodotto non approvato - è riportato un avviso fondamentale:
“Sono state segnalate gravi reazioni allergiche a seguito del vaccino Pfizer-BioNTech COVID-19 durante la vaccinazione di massa al di fuori degli studi clinici. Ulteriori reazioni avverse, alcune delle quali possono essere gravi, possono diventare evidenti con un uso più diffuso del vaccino Pfizer-BioNTech COVID-19 Vaccine.”
RISCHI COLLEGATI ALLA MANCANZA DI VALUTAZIONE DEI RISCHI CONNESSI AI MEDICINALI CONTENENTI OGM O DA ESSI COSTITUITI (DEROGA DELLE DISPOSIZIONI DELLA DIRETTIVA OGM)
Va rilevato che seppur molti esperti mettano in guardia sulla possibilità teorica che si possa verificare una retrotrascrizione da mRNA a DNA, ovvero segnalano l’eventualità che il nostro genoma possa subire una mutazione, e al di là di ogni eventuale e non trascurabile impatto sulla salute e sull’ambientale, lo scorso luglio, su proposta della Commissione europea approvata dal Parlamento, il Consiglio Europeo ha emanato un Regolamento54 che deroga “per il periodo durante il quale la pandemia di Covid-19 è considerata un'emergenza sanitaria pubblica, da alcune disposizioni della direttiva OGM per le sperimentazioni cliniche dei farmaci destinati a trattare o prevenire la Covid-19 (e anche per i trattamenti contro la Covid-19) contenenti OGM o da essi costituiti. La deroga proposta è applicata alle operazioni necessarie nella fase di sperimentazione clinica e nell'uso compassionevole o di emergenza nel contesto della pandemia di Covid-19.”
Nel Piano per la gestione del rischio (RMP) si legge:
“Non sono stati condotti studi di farmacologia di sicurezza, genotossicità e cancerogenicità, in conformità con la linea guida dell'OMS per i vaccini del 2005”.
E ciò nonostante EMA nel 2001 abbia pubblicato una guida agli studi di farmacologia di sicurezza55 rilevando che “si applica generalmente alle nuove entità chimiche e ai prodotti derivati dalla biotecnologia per uso umano”.
Anche nel RCP è indicato che “Non sono stati condotti studi di genotossicità o sul potenziale cancerogeno” seppur si legga poi:
“Si ritiene che i componenti del vaccino (lipidi e mRNA) non presentino alcun potenziale genotossico.”
Il verbo “ritenere” non può che esprimere ipotesi, dubbio, previsione e NON certezza. Tanto è vero che la tecnologia mRNA, fino a oggi NON è mai stata oggetto di licenza da parte delle Autorità regolatorie e pertanto NON è mai testata in condizioni reali e su vasta scala.
RISCHI COLLEGATI ALLA MANCANZA DI DATI RELATIVI A CRITICITÀ RILEVANTI SOTTO IL PROFILO DELLLA SICUREZZA, OGGETTO DI SPECIFIC OBLIGATION PER IL TITOLARE DELLA AUTORIZZAZIONE ALL’IMMISSIONE IN COMMERCIO CONDIZIONATA (CMA):
Si legge nel Rapporto pubblico di valutazione (EPAR public Assessment report) del trattamento Comirnaty di Pfizer-BioNTech56:
- “I dati (forniti, NdR) dimostrano la presenza di forme troncate/modificate di mRNA a livelli un po' più elevati nei lotti prodotti con il processo commerciale rispetto al materiale utilizzato negli studi clinici. Queste forme non sono sufficientemente caratterizzate e, sebbene i limitati dati forniti per l'espressione della proteina non affrontino completamente le incertezze relative al rischio di tradurre proteine/peptidi diversi dalla proteina spike prevista, si prevede che la quantità di tali proteine sia troppo bassa per suscitare una risposta immunitaria di rilevanza biologica. Dovrebbero essere forniti i dati di caratterizzazione delle proteine/peptidi rilevanti per le specie predominanti.”
- Deve essere valutata qualsiasi omologia tra le proteine tradotte (diverse dalla proteina spike prevista) e le proteine umane che, a causa del mimetismo molecolare, possono potenzialmente causare un processo autoimmune.
7.5.QUESITI APERTI
La tutela della salute individuale non può prescindere dal diritto a trattamenti accertati attraverso rigorosi percorsi di sperimentazione secondo criteri etici e metodologici.
|
SULL’IPOTESI DI UNA PROFILASSI SPERIMENTALE
|
Alla luce di quanto sopra riportato, si può dedurre che le conferme relative a tollerabilità, efficacia e sicurezza di Comirnaty, potrebbero trovare risposta soprattutto nelle attività di vigilanza post-autorizzazione (attiva e passiva), ovvero durante l’uso reale del farmaco m-RNA COVID-19, ovvero durante gli studi osservazionali di fase 4, quando è ancora in corso lo studio clinico di fase 3. Considerati gli importanti rischi identificati e potenziali, nonche’ quelli ad oggi sconosciuti, considerato che la sicurezza a lungo termine del trattamento Comirnaty e’ attualmente sconosciuta, considerato che il profilo di sicurezza di Comirnaty in casi specifici come gravidanza o immunodeficienza non è noto, è possibile affermare che stiamo prestando un consenso ad una sperimentazione? |
|
SULLA FARMACOVIGILANZA E LA COPERTURA ASSICURATIVA IN CASO DI REAZIONE AVVERSA
|
Quali sono le garanzie che il datore di lavoro offre a copertura del rischio di reazione avversa in caso di somministrazione di Comirnaty.? Quali sono le misure messe in atto all’interno del DVR per attuare una corretta ed efficace sorveglianza sanitaria se si dovesse accusare nell’arco dei successivi 24 mesi (la relazione finale dello studio cardine dovrà essere presentata entro dicembre 2023), - ovvero fino all’autorizzazione del trattamento secondo la standard marketing authorization - una reazione avversa, anche grave e finanche il decesso? Quali sono infine le misure di tutela assicurativa a garanzia che il sottoscritto, o la sua famiglia, sarà adeguatamente risarcito per i danni sofferti? |
|
SUL RISCHIO DI ANAFILASSI |
Per poter valutare al meglio il rischio di incorrere in un evento di anafilassi, trattandosi di un evento potenzialmente mortale, è necessario conoscere i dati aggiornati sulle segnalazioni di questa reazione avversa a Comirnaty in Europa e nel mondo e, possibilmente, con indicazione dei casi con storia di grave reazione allergica. A tale proposito è necessario valutare, preventivamente ad ogni profilassi, la titolazione anticorpale (anti PEG): come intende il datore di lavoro e il medico competente operare in questo senso nel DVR e nella sorveglianza sanitaria? |
|
SUL RISCHIO DI VAED E VAERD |
Poichè l’importante rischio potenziale “vaccine-associated enhanced disease (VAED), inclusa la vaccine-associated enhanced respiratory disease (VAERD), rappresenta uno degli scenari di rischio a medio-lungo termine è necessario valutarlo nel bilanciare correttamente il rapporto rischi/benefici della profilassi. Si chiede di avere evidenza della valutazione di questo rischio. |
|
SUI RISCHI DI PROFILASSI PER LE DONNE IN STATO DI GRAVIDANZA E/O IN ALLATTAMENTO |
Per poter valutare al meglio il rischio, è necessario conoscere i dati aggiornati su eventuali segnalazioni di reazione avversa a Comirnaty in donne in stato di gravidanza (o in bambini allattati con latte materno). |
|
SUI RISCHI DI PROFILASSI PER I SOGGETTI IMMUNOCOMPROMESSI |
Per poter valutare al meglio il rischio è necessario conoscere i dati aggiornati su eventuali segnalazioni di reazione avversa a Comirnaty in soggetti immunocompromessi. Poiché l'efficacia del farmaco può essere inferiore negli individui immunocompromessi, diminuendo così la loro protezione da covid-19, è necessario conoscere i dati aggiornati sull’efficacia per bilanciare correttamente il rapporto rischi/benefici della profilassi. Quanto può essere “informato” un consenso a un trattamento se non è noto il profilo di sicurezza né l'efficacia né tantomeno le possibili reazioni avverse? |
|
SUI RISCHI DI PROFILASSI PER I SOGGETTI FRAGILI CON COMORBILITA’ |
Per poter valutare al meglio il rischio è necessario conoscere i dati aggiornati su eventuali segnalazioni di reazione avversa a Comirnaty in soggetti fragili con comorbilità. Quanto può essere “informato” un consenso a un trattamento se non è noto il profilo di sicurezza né le possibili reazioni avverse? |
|
SUI RISCHI DI PROFILASSI PER I SOGGETTI CON DISTURBI AUTOIMMUNI O INFIAMMATORI |
Per poter valutare al meglio il rischio è necessario conoscere i dati aggiornati su eventuali segnalazioni di reazione avversa a Comirnaty in soggetti con disturbi autoimmuni o infiammatori. Quanto può essere “informato” un consenso a un trattamento se non è noto il profilo di sicurezza né le possibili reazioni avverse? |
8.CONSIDERAZIONI SULLA VALUTAZIONE DEL RISCHIO
8.1.LETALITA’ E MORTALITA’
Al fine di ponderare al meglio rischi e benefici è fondamentale conoscere l'“aggressività del virus”. La letalità del virus viene calcolata su quante persone positive si aggravano a tal punto da morire.
Lo scorso 19 gennaio, in uno dei suoi interventi al Senato, il presidente del Consiglio Giuseppe Conte ha menzionato il Prof. Massimo Galli, primario del reparto Malattie Infettive dell’ospedale Sacco di Milano:
“Di recente un illustre infettivologo dell’ospedale Sacco di Milano, il professor Galli, ha detto che se prendiamo i dati nel periodo tra settembre e gennaio in Italia abbiamo il 2% circa della letalità tra i casi confermati”.
È chiaro che qualsiasi misura non riuscirebbe a tenere in debita considerazione l’eterogeneità fra i diversi gruppi di popolazione, la loro distribuzione e i relativi rischi: tuttavia l’OMS si è spinta ad affermare lo scorso ottobre che il coronavirus avrebbe colpito il 10% della popolazione mondiale, pertanto – in base ai dati disponibili - la letalità potrebbe risultare circa quattro volte più bassa, quasi pari a quella dell’influenza57. Ad oggi sembra quindi che non siamo in grado di determinare con precisione il reale tasso di letalità di Covid-19.
Tuttavia, l’idea che il covid-19 sia lo stesso problema sanitario per tutto il mondo, e che si possa facilmente generalizzare da un Paese, o addirittura da un continente, all’altro è radicalmente sbagliata (Prof. Mamone Capria58).
Riportiamo di seguito alcune considerazioni che sono fondamentali per costruire un quadro più comprensibile dell’impatto Covid-19 in termini di Mortalità e Letalità, con particolare riferimento al territorio nazionale ma con cenni anche a situazioni internazionali.
Sul fatto che, oltre ogni ragionevole dubbio, il carattere altamente specifico da un punto di vista geopolitico della cosiddetta “pandemia virale” sia un dato assodato non c’è alcun dubbio.
Prendiamo ad esempio l’Africa: tra i problemi cronici dell’Africa c’è la carenza numerica e qualitativa delle sue strutture igieniche e sanitarie. In particolare, ha pochi medici e poco personale sanitario. In Africa nel 2016 si registravano 416.000 morti per tubercolosi (una tragedia sanitaria di cui nessun media mainstream parla). Nella prima metà del 2020 gli “esperti” prevedevano che, tra tutti i continenti, sarebbe stata quello più martoriato dalla pandemia, e la stima che un modello matematico predittivo per l’Africa forniva era di circa 150.000 decessi per Covid-19 nel solo primo anno di pandemia.
Bene, al 20 dicembre 2020, la percentuale dei casi di covid-19 e la percentuale dei decessi attribuiti al covid-19 sono state, in entrambi i casi, il 2% rispetto ai valori mondiali di entrambi. E in Africa ci sono stati 37.741 decessi attribuiti al covid-19, cioè meno della metà del valore minimo previsto.
In Italia, un paese industriale, con standard sanitari incomparabili a quelli medi africani e con circa 1/18 della popolazione dell’Africa, ci sono stati, secondo la stima ufficiale aggiornata al 28 dicembre dell’ISS, 70.085 morti “covid-19”, cioè ha avuto quasi il doppio dei morti attribuiti al covid-19 in “Africa”.
Inoltre, l’Italia ha avuto il 13% dei morti in tutta Europa e la mortalità massima tra i paesi europei, nonostante i severissimi provvedimenti restrittivi («lockdown») che è stata tra i primi Paesi ad adottare.
Lo scorso 30 dicembre l'Istituto nazionale di statistica (ISTAT), congiuntamente all’Istituto Superiore di Sanità (ISS), ha presentato un’analisi della mortalità nel periodo gennaio-novembre 202059.
“Nel periodo di osservazione dell’epidemia di Covid-19 (febbraio-novembre 2020) si stimano complessivamente circa 84 mila morti in più rispetto alla media del 2015-2019”, per lo più verificatesi nella classe di età da 80 anni in poi. Tuttavia, in questa analisi, si legge anche che “per quanto riguarda la classe di età 0-49 anni, per quasi tutto il periodo considerato i decessi mensili del 2020 sono inferiori a quelli medi del 2015-2019.”
Se si analizzano in dettaglio i dati dei decessi negli ultimi sei anni60, si nota che rispetto all’anno 2015 (quello con mortalità più alta negli ultimi 5 anni) nel 2020 (oltretutto il dato del mese di novembre è stimato) si registrano circa 64.000 (+11%) decessi in più nel 2020. L’andamento di questo eccesso di mortalità si caratterizza però da una forbice piuttosto ampia fra nord-centro-sud Italia: infatti al nord Italia l’aumento percentuale è del 20% circa, mentre al centro è del 3% come al sud, 3%.
Inoltre, il fenomeno, sempre in termini di eccesso della mortalità, è sostanzialmente concentrato in poche provincie italiane, la maggior parte della Lombardia e nelle Marche e in un periodo molto limitato dell’anno, ovvero nel periodo che va da fine febbraio ai primi di maggio 202061.
L’impatto della mortalità “covid-19” dovrebbe essere stato un fenomeno coerente nel tempo e per l’intera popolazione italiana (così interconnessa in termini di circolazione di merci, lavoratori e turisti), che tale disparità semplicemente non si può spiegare in termini dell’azione di un singolo agente contagioso.
Come si vede dai dati pubblicati da “epicentro” nel bollettino del 16 dicembre 202062, la Lombardia, che ha il 16% della popolazione italiana, ha visto da sola il 37,9% dei decessi; e Lombardia, Piemonte ed Emilia-Romagna, che formano il 31% della popolazione italiana, hanno visto insieme il 57,2% dei decessi.
Invece Campania, Puglia, Basilicata, Calabria e Sicilia, che formano il 28,5% della popolazione italiana, hanno visto insieme l’11,3% dei decessi!
Cambiamo per un momento prospettiva geopolitica e spostiamoci in Tanzania. La Tanzania è un paese africano molto povero e con 45 milioni di abitanti.
Il suo presidente si è rifiutato di bloccare l’economia in funzione di contrasto al covid-19 e per questa ragione è stato trattato come un pazzo criminale dalle autorità sanitarie, dai principali media e dagli “esperti”. Eppure, secondo l’OMS al 20 dicembre i morti tanzaniti con covid-19 erano stati … 21.
È rilevante evidenziare che la Procura di Bergamo indaga per epidemia colposa e falso63. Tutto è partito dall’indagine di omicidio colposo in relazione alle denunce presentate il 10 giugno dai familiari delle persone morte per coronavirus che fanno parte del Comitato “Noi denunceremo”.
Sotto il profilo epidemiologico, parrebbe utile valutare la media dei decessi per tipo di malattia confrontando gli stessi periodi degli anni precedenti: non è ancora possibile farlo con i dati italiani, ma possiamo analizzare nel frattempo quelli pubblicati dall’istituto di statistica inglese (l’ONS64). Quello che si nota chiaramente è una sensibile regressione delle altre cause rispetto all’emergere della mortalità collegata al Covid-1965. Tra le situazioni emblematiche spicca il caso dell’influenza stagionale che sembrerebbe sostanzialmente “molto ridimensionata”, così come anche alle nostre latitudini66.
Il covid-19 è, a tutti gli effetti, una sindrome SIMILINFLUENZALE che è stata dichiarata all’OMS, dal governo cinese il 31 dicembre 2019 e identificata l’8 gennaio 2020 come dovuta a un coronavirus denominato SARS-CoV-267.
È dalla Cina che si sarebbe diffusa nei paesi europei, arrivando in Italia a febbraio.
Questa versione dei fatti è stata quella ufficiale per diversi mesi, ma oggi sappiamo che in Italia il SARS-CoV-2 era in circolazione almeno da novembre68.
Ma che cosa sappiamo del SARS-CoV-2stesso e della sua relazione con il Covid-19?
Questa distinzione non è solo importante sotto il profilo scientifico, ma anche a livello di interventi sanitari. Se il cov-2 (virus) è la causa del covid-19 (sindrome SIMILINFLUENZALE), allora
(1) identificare e isolare i contagiosi e
(2) prevenire il contagio
è una strategia scientificamente fondata per evitare il dilagare dell’epidemia.
Tuttavia, anche assumendo certa la relazione causale tra cov-2 e covid-19, l’effettivo impatto del covid-19 sulla mortalità in una certa popolazione dipenderebbe da:
(3) le condizioni individuali, epidemiologiche e sanitarie che favoriscono l’insorgenza di complicanze;
(4) la capacità di curare le complicanze del covid-19.
È solo se ci si dichiara incapaci di intervenire sulle condizioni (3), e se si nega (4) come si è fatto sistematicamente (cioè si dichiara invalida ogni terapia proposta anche se dimostrata si efficace sul campo) che la strategia (1)-(2) assume la centralità che in questi mesi il governo italiano ed altri governi le hanno conferito.
Prendiamo adesso un rapporto recente dell’ISS69. Secondo tale rapporto, al 22 dicembre in Italia ci sono stati 1.963.023 «casi», e 67.540 «deceduti». La «letalità» è il rapporto 67.540/1.963.023, ovvero circa 3,4%.
Ma che cos’è un “caso”?
Andando in un’altra pagina dell’ISS si legge: https://www.epicentro.iss.it/coronavirus/sars-cov-2-sorveglianza-dati
«Si ricorda che la definizione internazionale di caso, adottata anche dall’ISS, prevede che venga considerata come caso confermato una persona con una conferma di laboratorio del virus che causa COVID-19 a prescindere dai segni e sintomi clinici.»
Quindi la definizione utilizzata dall’ISS è in conflitto con le indicazioni (per quanto tardive) dell’OMS sopra citate: un «caso» nel senso dell’ISS è un individuo positivo al tampone, senza la contestualizzazione che l’OMS ritiene indispensabile a dargli un significato clinico.
A partire dal 23 aprile nelle statistiche della Protezione Civile, oltre al totale dei tamponi effettuati, c’è anche una nuova colonna dei “casi testati”, in cui figurano numeri nettamente più bassi.
Così fino al 22 dicembre i tamponi effettuati sono stati 25.383.219, ma le persone testate sono state solo 14.386.848.70
Ora i “casi” sono stati 1.301.573, quindi il 9% degli individui testati è stato positivo in un qualche momento tra febbraio e dicembre del 2020: 1.301.573/14.386.848 = 9,05%
Come mai l’OMS si è finalmente sbilanciata? Perché non aveva spiegato il rischio di falsi positivi molto prima? Una spiegazione plausibile è che regole più stringenti per la diagnosi del Covid-19, in corrispondenza dell’inizio della campagna vaccinale, permetteranno di diminuire i falsi positivi e attribuire tale diminuzione al vaccino.
Non sarebbe la prima volta che il successo di una campagna di vaccinazioni è stato realizzato cambiando definizioni chiave e criteri diagnostici da prima a dopo l’inizio della campagna. Forse l’esempio più famoso è quello del cambiamento della definizione di epidemia e di poliomielite da prima a dopo l’introduzione del vaccino Salk.
Relativamente ai “casi” occorre fare una distinzione importante: normalmente in medicina un “caso” di una certa malattia è una persona malata. Ma così non è con i “casi” di covid-19: in breve, tra i casi di covid-19 il malato non è la regola, ma l’eccezione.
Notiamo innanzitutto la fine distinzione che si è tracciata tra gli stati di non-malattia tra i positivi:
- l’asintomatico (non ha sintomi e non li avrà mai);
- il presintomatico (non ha sintomi, ma li avrà (?) entro un massimo di 14 giorni);
- il paucisintomatico (ha “pochi” (?) sintomi);
- il lievemente sintomatico.
A queste categorie di non-malattia fanno seguito i casi di malattia, distinti tra severi e critici.
Che l’asintomatico sia contagioso è qualcosa che si continua a ripetere ma, ad oggi, non esistono prove convincenti che questo sia vero. E nemmeno esistono test di infettività in uso corrente che possano stabilirlo in un caso particolare.
Per capire quale sia l’incidenza delle prime 4 classi rispetto alle altre 2 basta guardare il seguente grafico, aggiornato al 30 novembre.
È chiaro che dal mese di luglio in poi i casi severi o critici formano meno del 5%.
Per considerare il periodo successivo, nei 30 giorni fino al 22 dicembre ci sono stati 490.197 casi, e circa 24.510 sono stati severi o critici.
Se consideriamo che il 9% della popolazione italiana sono stati “casi” tra febbraio e dicembre, ma meno del 5% di questi hanno avuto bisogno del ricovero in ospedale, si ricava che nello stesso periodo il rischio di essere ospedalizzati in un reparto covid-19 è stato lo 0,45%, cioè 1 su 2222 (dati epicentro, bollettino del 22 dicembre).
8.2.Distribuzione della gravità dei casi di Covid-19
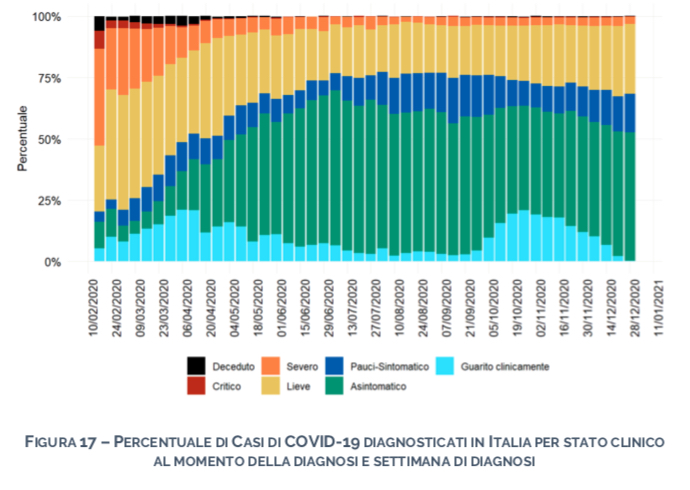
Approfondendo il tema dei decessi per Covid-19, anche ammettendo che l’attribuzione al covid-19 dei decessi censiti dall’Istituto Superiore di Sanità (ISS) non dia adito a dubbi, il dato di gran lunga più importante per farsi un’idea realistica del covid-19 riguarda le età degli individui censiti.
Secondo il rapporto covid-19 aggiornato al 16 dicembre71, l'età mediana dei deceduti positivi è 82 anni, mentre quella dei positivi è inferiore di più di 30 anni: 48 anni.
In Italia l'aspettativa di vita alla nascita è 85,3 anni per le donne e 81,0 per gli uomini.
Ora, in base alla stessa fonte, l’età mediana dei morti per covid-19 è, per le donne, 85 anni, e per gli uomini 80. In prima approssimazione, ciò indica che il covid-19 uccide prevalentemente soggetti vicini al limite della loro aspettativa di vita.
Questo non significa che queste morti siano semplicemente accettabili ma il contesto va considerato nel quadro generale se si vuole ragionare in termini di valutazione del rischio.
Piuttosto è vero il contrario, ovvero, il fatto che nelle residenze per anziani c' è stata un'alta proporzione dei morti "per covid-19" è solo una delle tante prove che si è molto lontani dal curarsi degli anziani come si dovrebbe.
Collegare la mediana dei decessi all’aspettativa di vita ci dà quindi una parte di un’importante verità sul covid-19.
Ma non tutta. L’altra parte è che i morti “covid-19” con almeno una grave patologia preesistente costituiscono il 96,9%, e quelli che ne hanno almeno 3 (sic!) sono il 66,2%.
Quindi l’enunciato completo è:
“il Covid-19 uccide prevalentemente soggetti vicini al limite della loro aspettativa di vita e, per tutte le fasce d’età, sofferenti di una o, per la maggioranza, più di 3 gravi patologie croniche. Questa è la realtà dei fatti epidemiologici."
Il dato viene confermato dal Report Covid dell’ISS del 16 dicembre 2020:
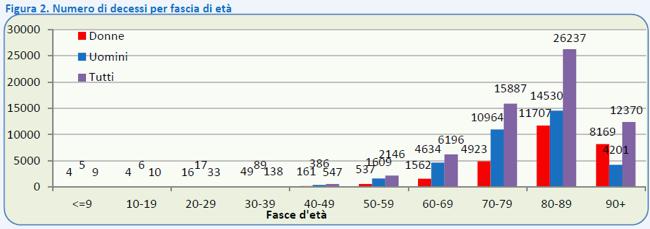
Fino a 50 anni non compiuti i morti “positivi” sono stati 737 su un totale di 63.562, cioè l’1,1%. Di questi 737, erano solo 19 quelli che «non avevano diagnosticate patologie di rilievo».
L'età media in Italia è 45,7 anni. La popolazione fino a 50 anni non compiuti è il 55,3% della popolazione, cioè 33,35 milioni. Quindi nella fascia d'età fino a 49 anni compiuti la mortalità del covid-19 è stata: 737/33.35 x 10-6 = 22 milionesimi, cioè lo 0,0022%, o, se si preferisce, 2,2 su 100.000.
Pertanto, dire che chi ha meno di 50 anni, e anche chi ne ha molti di più ma non soffre di gravi patologie croniche, non debba preoccuparsi eccessivamente del covid-19, non è frutto di un irresponsabile ottimismo che “nega” che ci siano stati morti, ma è una sintesi oggettiva del quadro fornito dai dati epidemiologici ufficiali.
È chi nega questo, che sta negando le evidenze epidemiologiche ufficiali.
In questi mesi siamo stati informati, giorno per giorno, dei morti da covid-19: ogni giorno viene comunicato il numero dei nuovi casi e il numero delle vittime.
Ora, innanzitutto la mediana, nei casi fatali, tra l’insorgenza dei sintomi e il decesso è 12 giorni: quindi l’accostamento dei nuovi casi alle vittime è in sé stesso privo di senso statistico.
Se in un giorno c’è una diminuzione dei nuovi casi, non dobbiamo aspettarci per quel giorno anche una diminuzione delle vittime, perché queste saranno comprese tra i casi, per ipotesi più numerosi, di 2 settimane prima.
Inoltre, i casi, di per sé, hanno senso solo se si riporta il tasso dei positivi rispetto alle persone testate.
La positività rispetto al totale dei tamponi effettuati si è attestata intorno al 7,8%.
Questo non vuol dire che attualmente il 7,8% della popolazione sia positiva, ma è la percentuale degli italiani che, sottoposti al tampone in qualche momento tra febbraio e dicembre 2020, lo sono stati.
Al 26 dicembre la percentuale della popolazione italiana che è positiva è stimata essere lo 0,9%.
8.3.L’andamento della mortalità negli ultimi anni
Ma i decessi giornalieri per Covid-19 (qualora validati) sono tanti o pochi?
La media della mortalità quotidiana negli ultimi 5 anni è stata 1728.
Se si va a guardare l’evoluzione della mortalità in Italia negli ultimi anni, si scopre che è in costante crescita da ben dieci anni. Ecco il grafico del tasso di mortalità ogni 1000 persone in Italia dal 2000 al 202072:
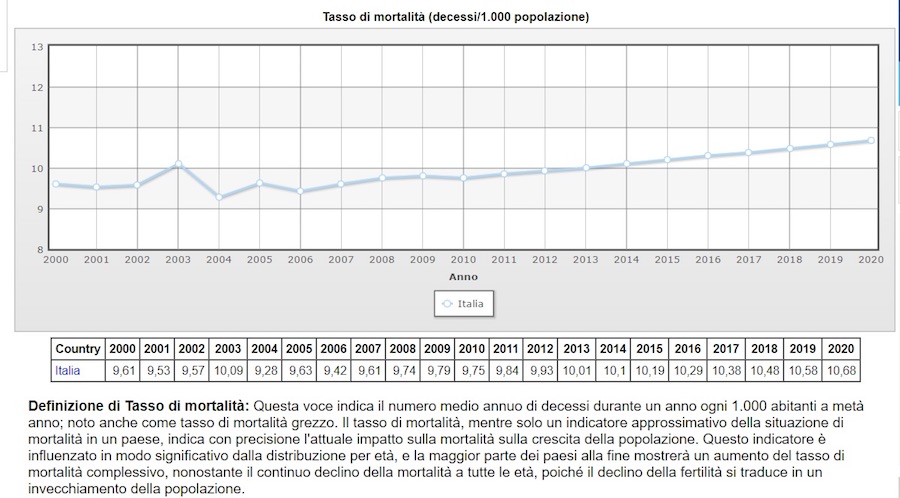
A partire dal 2010 tra il numero di anni e il tasso c’è una correlazione lineare pressoché perfetta, e si vede che il tasso di decessi per 1000 cresce di 1/10 ogni anno. Inutile dirlo, nessuno dei principali media ha mai parlato di questa crescita oggettiva della mortalità per tutte le cause.
Questo grafico mostra chiaramente che siamo di fronte a un regresso sanitario non su 10 mesi, ma su 10 anni, e che il covid-19 vi ha avuto un ruolo da comprimario, non da protagonista. Ancora una volta: i morti sono reali, dolorosamente e innegabilmente reali.
Quello che non è reale è il ruolo ingigantito attribuito all’infezione da SARS Cov-2. Chi ne ha fatto un’emergenza in nome della quale nessuna rinuncia, nemmeno al lavoro e ai diritti civili, era eccessiva, avrebbe dovuto spiegare prima questo fenomeno di lungo periodo.
Nessuno l’ha fatto. Ci sono ipotesi verosimili per questa crescita del tasso di mortalità, e anche molto probabili. Innanzitutto, è evidente che il depotenziamento della sanità pubblica ha concorso a questa tendenza.
Ma ci sono altre ragioni:
Inquinamento atmosferico: L’Italia è da anni oggetto di procedure d’infrazione per violazione dei parametri della salubrità dell’aria. L’ultima sentenza di condanna dell’Italia da parte della Corte di giustizia europea è del 10 novembre 2020, e riguarda il «superamento sistematico e continuato dei valori limite applicabili alle microparticelle (PM10) in determinate zone e agglomerati italiani» (per un’analisi si veda73.
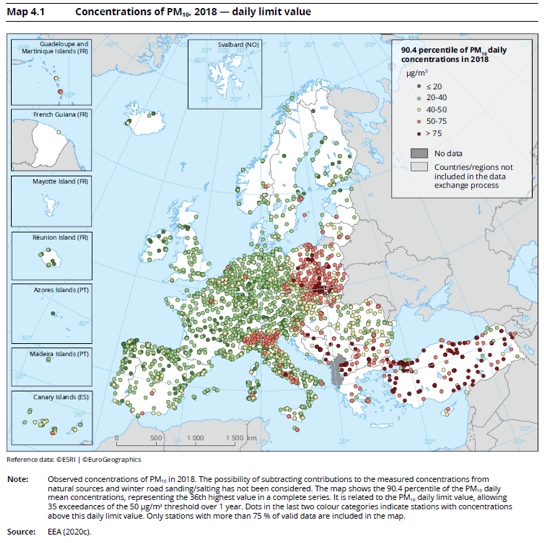
In Italia, i dati disponibili mostrano che il valore limite per il Pm2,5 non è stato rispettato dal 2015 in diverse città della Pianura Padana, tra cui in particolare Venezia, Padova e varie zone vicine alla città di Milano. Il Pm10 e il Pm2,5 sono particolarmente pericolosi per la salute umana. L’esposizione al particolato può influire sulla funzione polmonare e causare, o aggravare, malattie cardiovascolari e respiratorie, infarti e aritmie; inoltre può avere conseguenze per il sistema nervoso centrale e il sistema riproduttivo, e provocare il cancro. E a questo proposito, le province in cui, nonostante tutte le misure di isolamento dal “contagio”, la mortalità attribuita al covid-19 ha raggiunto e mantenuto i massimi livelli sono esattamente quelle maggiormente colpite dall’inquinamento atmosferico delle aree urbane.74
Secondo i report della EEA (Agenzia europea dell’ambiente), Report 2020, la pianura padana, ad esempio, è una delle regioni europee più critiche per la concentrazione di PM10.75
Secondo epicentro76 l’Italia è il Paese con il maggior numero di morti per inquinamento ambientale in Europa.
Le morti per SIMILINFLUENZE e loro complicanze. Il complesso delle SIMILINFLUENZE ha mietuto in stagioni influenzali recenti (2013-2017) una media di 34.000 vittime per anno, mentre l’ISS continua a riportare, parlando solo dell’influenza in senso stretto (e nemmeno per la sola influenza questo è vero!) che si tratterebbe di ... 8000 morti.
Molti “esperti” avevano previsto che all’arrivo dell’autunno le forze riunite della normale “influenza” (tenere presente che molto spesso si legge “influenza” ma bisogna intendere SIMILINFLUENZA) e della seconda ondata del Covid-19 avrebbero messo in crisi qualsiasi resistenza sanitaria.
Altri studiosi avevano invece congetturato che il Covid-19 non fosse che una componente del complesso delle SIMILINFLUENZE, che aveva semplicemente assorbito a livello diagnostico le sue consorelle – e anche varie altre malattie che la fallibilità e l’abuso dei tamponi gli aveva erroneamente accreditato.
Bene: in data 24 ottobre è apparso su un quotidiano un articolo dal titolo: «L’influenza è stata ammazzata dal covid?77
Basta dare un’occhiata al grafico della stagione SIMILINFLUENZALE 2020-21 per capire che anche in Italia il covid-19 sta rubando la scena alle SIMILINFLUENZE:78
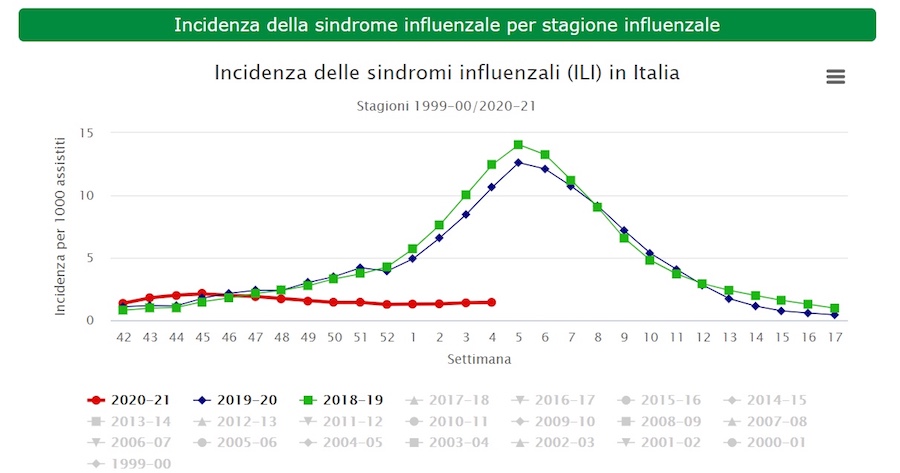
Leggiamo dal rapporto79:
Rapporto N. 11 del 3 febbraio 2021, Stagione Influenzale 2020 – 2021: la popolazione degli assisti in sorveglianza è mediamente pari a 1.449.694 assistiti per settimana (range: 909.330 — 1.554.039) pari al 2,4% dell’intera popolazione italiana … Nella quarta settimana del 2021 la curva epidemica delle sindromi SIMILINFLUENZALI è stabile e sotto la soglia epidemica. Nella scorsa stagione in questa stessa settimana veniva raggiunto il picco epidemico stagionale e il livello di incidenza era pari a 12,6 casi per mille assistiti contro 1,4 di questa stagione.
Le infezioni ospedaliere. Una piaga endemica del sistema ospedaliero italiano sono le infezioni che si contraggono in molti reparti. Nel 2016 tra infezioni ospedaliere ed esposizione a tre inquinanti dell’aria (e non sono i soli!) che hanno portato l’Italia di fronte alla Corte di Giustizia europea, sono morti 125.501 cittadini: 1,8 volte i morti attribuiti al covid-19 in questo 2020.
Nessun presidente del consiglio aveva dichiarato lo stato di emergenza, nessun telegiornale ne aveva dato notizia con un minimo di enfasi e di attenzione continuativa, l’economia non era stata bloccata, le scuole erano rimaste aperte anche nelle città più notoriamente inquinate, e ovviamente nessuno ci informava quotidianamente su quanti erano morti anche solo per queste due cause – la seconda delle quali poteva essere esattamente monitorata sulla base delle cartelle cliniche.
La cattiva gestione delle RSA. Nella conferenza stampa del 12 dicembre, il Presidente del Consiglio Conte ha dato, come una delle spiegazioni della maggiore mortalità da covid-19 in Italia, la seguente:
«dipende anche dalle abitudini di vita, è risaputo che in Italia siamo un paese in cui gli anziani di solito li teniamo vicino a noi»,
e poi ha accennato in maniera confusa (probabilmente per timore di provocare un incidente diplomatico) alle «diverse abitudini di vita» di «altri Paesi».
È difficile dire dove questa risposta sia più sbagliata:
- nel suggerimento che in Italia le persone anziane siano morte prevalentemente perché contagiate a casa da figli e nipoti, o
- nell’assunto che gli italiani non mandano i loro anziani in ospizi e RSA?
Eppure, dovrebbe essere «risaputo» che nel 2020 le residenze per anziani, in Italia, sono state un luogo di massima diffusione del covid-19, e al 6 aprile era da lì che derivavano più della metà dei decessi attribuiti al covid-19. Invece di indulgere alla retorica si poteva cogliere l’occasione per biasimare i responsabili della cattiva gestione delle RSA, compresa la sconcertante decisione dell’assessore al Welfare della Lombardia di trasferirvi i convalescenti del covid-19.
Gli interventi mancati. Ci sono poi i decessi dovuti agli oltre 700.000 interventi e visite ospedaliere che sono stati rinviati perché si dovevano requisire per il covid-19 interi reparti. Questa situazione era stata denunciata anche da alcuni medici.
Ecco una recente stima (19 dicembre):80
«Da chi soffre di bronchite a chi ha insufficienza renale o cardiaca, sono quasi 700.000, solo nei reparti di Medicina interna, le persone che hanno subìto gli effetti indiretti del Covid, vedendo saltare il ricovero a causa della pandemia. E, a esser penalizzati, sono soprattutto i malati cronici: a quasi 400.000 non è stata garantita assistenza ospedaliera. […]»
A questo bisogna aggiungere i decessi dovuti ai ritardi nei ricoveri urgenti dovuti o ad ambulanze che non sono arrivate81 o all’attesa, per ore, dei risultati del tampone.
Le indicazioni fuorvianti date a medici ospedalieri e di base. I medici ospedalieri erano stati sconsigliati dal ministero della Salute di effettuare autopsie, ed erano stati indotti a curare come polmoniti quelle che erano tromboembolie. In molti casi l’errore diagnostico è stato fatale al “paziente covid”.
Contemporaneamente, i medici di base sono stati sconsigliati dal visitare i propri pazienti, ma quelli che hanno disobbedito sono riusciti a far attraversare senza vittime tra i loro assistiti l’intera crisi covid-19. Vale la pena citare un lungo stralcio della testimonianza della dottoressa Maria Grazia Dondini82:
«Il 22 febbraio di quest’anno è stata comunicata la circolazione di un nuovo coronavirus. Il Ministero della Salute ha mandato un’ordinanza a tutti noi medici del territorio, dicendoci sostanzialmente che eravamo di fronte a un nuovo virus, sconosciuto, per il quale non esisteva alcuna terapia.
La cosa paradossale è che fino a quel giorno avevamo gestito i medesimi pazienti con successo, senza affollare ospedali e terapie intensive; ma da quel momento si è deciso che tutto quello che avevamo fatto fino ad allora non poteva più funzionare. Non era più possibile un approccio clinico/terapeutico.
Noi, medici di Medicina generale, dovevamo da allora delegare al dipartimento di Sanità Pubblica, che non fa clinica, ma una sorveglianza di tipo epidemiologico; potevamo vedere i pazienti solamente se in possesso di mascherina FFP2, che io ho potuto ritirare all’ASL solo il 30 di marzo.
Ma c’è una cosa più grave.
Nella circolare ministeriale, il Ministro della Sanità ci dava le seguenti indicazioni su come approcciarci ai malati: isolamento e riduzione dei contatti, uso dei vari DPI, disincentivazione delle iniziative di ricorso autonomo ai servizi sanitari, al pronto soccorso, al medico di medicina generale.
Dunque, le persone che stavano male erano isolate; e, cosa ancora più grave, il numero di pubblica utilità previsto non rispondeva.
In sintesi: le polmoniti atipiche non sono state più trattate con antibiotico, i pazienti lasciati soli, abbandonati a sé stessi a domicilio.
Ovviamente dopo 7-10 giorni, con la cascata di citochine e l’amplificazione del processo infiammatorio, arrivavano in ospedale in fin di vita. Poi, la ventilazione meccanica ha fatto il resto.»
In un Paese normale una testimonianza di questo genere avrebbe costretto alle immediate dimissioni il ministro della Salute e i suoi consulenti «tecnico-scientifici».
9.I TRATTAMENTI POSSIBILI DEL COVID-19
È rilevante evidenziare che la Procura di Bergamo indaga per epidemia colposa e falso83. Tutto è partito dall’indagine di omicidio colposo in relazione alle denunce presentate il 10 giugno dai familiari delle persone morte per coronavirus che fanno parte del Comitato “Noi denunceremo”.
Lo scorso 30 novembre 2020 il ministero ha fornito indicazioni operative per la gestione a domicilio del caso a partire dalla diagnosi84 emanando la Circolare85 "Gestione domiciliare dei pazienti con infezione da SARS-CoV-2"86, dove si può leggere:
“I dati di letteratura attualmente disponibili hanno evidenziato un’associazione significativa tra l’incidenza di forme clinicamente severe d’infezione da SARS-Cov2 e l’età avanzata (soprattutto oltre i 70 anni d’età), il numero e la tipologia di patologie associate, il sesso maschile e la latenza tra l’inizio dei sintomi e la prima valutazione medica”.
Il Prof. Marco Cosentino in un’intervista pubblicata lo scorso 12 gennaio afferma87:
“Si evidenzia senza ombra di dubbio un problema di natura organizzativa e strategica. Ad un anno ormai quasi compiuto dalla manifestazione della vicenda, le strutture e attività, nonché il modus operandi del sistema sanitario proseguono, tuttavia, come se l’emergenza fosse appena stata dichiarata. Ad esempio, la carenza di personale medico e sanitario e di posti letto negli ospedali – indiscutibilmente legata ai tagli degli ultimi decenni – costituisce un’emergenza nell’emergenza che ancora nessuno ha ritenuto di affrontare. Il contrasto tra i quotidiani richiami all’emergenza sanitaria e la mancanza fin qui di reali interventi strutturali si fa sempre più stridente. Non dobbiamo tra l’altro dimenticarci che le conseguenze di questa emergenza riguardano non solo i malati di Covid, bensì tutti gli altri malati di malattie altrettanto o più gravi, soprattutto croniche, e che si ritrovano reparti e ambulatori chiusi a causa del Covid”.
Si assiste purtroppo ad una discussione tecnica su come affrontare l’infezione da Covid-19 che tende a RIDURRE l’approccio metodologico a linee di intervento discrete, senza prendere in considerazione l’ampio contributo offerto da molti ambiti specialistici, quasi a favorire l’adozione di ben determinati provvedimenti, rinunciando in principio ad un approccio multidisciplinare al problema.
Questa tendenza e le relative “scelte di campo” effettuate dagli attori istituzionali non permettono una valutazione oggettiva delle possibili terapie preventive e di contrasto all’infezione, negando di fatto possibilità di cura e prevenzione che possono risultare determinanti nel contenimento dell’infezione88.
È noto89, ad esempio, che AIFA abbia bloccato lo studio sperimentale “Therapeutic effects of adenosine in high flowm 21% oxygen aereosol in patients with Covid19-pneumonia”, un trattamento ideato esperimentato presso il “Grande Ospedale Metropolitano di Reggio Calabria” dal professor Pierpaolo Correale, direttore dell’Unità operativa complessa di Oncologia, con il supporto del professor Sebastiano Macheda, direttore della Terapia intensiva ed Anestesia dello stesso ospedale.
Si tratta di una tecnica innovativa:
“l’adenosina viene introdotta in un aerogen, una specie di aerosol, che nebulizza l’adenosina e permette la somministrazione solo per via endobronchiale.”
Il trattamento in pazienti gravi si è rilevato di particolare efficacia, nonché privo di effetti collaterali: “in 48 ore, avevano risolto il problema respiratorio e, dopo una settimana, la polmonite era completamente risolta”.
Si legge nella risposta non favorevole di AIFA:
“in considerazione di un rapporto rischio/beneficio non definibile; si ritiene che a fronte dell’attuale disponibilità di alcune opzioni terapeutiche di provata efficacia lo studio proposto non possa essere autorizzato”.
Pur non conoscendo il razionale scientifico di una simile decisione da parte di AIFA, ciò che si apprende dalle testate giornalistiche è davvero allarmante, ovvero, in Italia, nonostante i bollettini dei decessi ogni giorno riempiano i titoli di cronaca, le criticità in termini di organizzazione e strategia del sistema sanitario siano sempre più evidenti, NON sono autorizzati studi sperimentali per terapie altamente promettenti in termini di efficacia e sicurezza anche per stadi avanzati della Covid-19.
Una decisione che appare certamente incomprensibile, dal momento che la risposta di AIFA è comunque emblematica: oggi ci sarebbe la disponibilità di alcune opzioni terapeutiche di provata efficacia.
9.1.QUESITI APERTI
|
SULLA DISPONIBILITÀ DI TRATTAMENTI TERAPEUTICI E DI PROFILASSI EFFICACI
|
Appare evidente che finché non saranno disponibili trattamenti di profilassi di indubbia efficacia e sicurezza, supportati da dati clinici sufficienti, autorizzati secondo una standard marketing authorization, si rende necessario poter valutare alternative a Comirnaty nell’ambito dell’attuale disponibilità di alcune opzioni terapeutiche di provata efficacia. |
Approfondimenti e citazioni bibliografiche
2 Il datore di lavoro deve adottare tutte le misure idonee a prevenire sia i rischi insiti all'ambiente di lavoro, sia quelli derivanti da fattori esterni e inerenti al luogo in cui tale ambiente si trova, atteso che la sicurezza del lavoratore è un bene di rilevanza costituzionale che impone al datore di anteporre al proprio profitto la sicurezza di chi esegue la prestazione.
3 https://www.trovanorme.salute.gov.it/norme/dettaglioAtto?id=77479&articolo=26
4 https://www.trovanorme.salute.gov.it/norme/dettaglioAtto?id=77479&articolo=26
5 vedi FAQ n.18 (https://www.aifa.gov.it/documents/20142/1279946/FAQ-Vaccinazione_anti_COVID-19_con_vaccino_Pfizer.pdf/ea9099cd-c71c-d443-e447-6da60137da37)
“Chi ha già avuto un’infezione da COVID-19, confermata, deve o può vaccinarsi?
La vaccinazione non contrasta con una precedente infezione da COVID-19, anzi potenzia la sua memoria immunitaria, per cui non è utile alcun test prima della vaccinazione. Tuttavia, coloro che hanno avuto una diagnosi di positività a COVID-19 non necessitano di una vaccinazione nella prima fase della campagna vaccinale, mentre potrebbe essere considerata quando si otterranno dati sulla durata della protezione immunitaria.”
7 http://www.salute.gov.it/imgs/C_17_pagineAree_5373_16_file.pdf
11 Fondamentale è quindi l’INFORMAZIONE, che deve essere:
- Personalizzata: Adeguata alla situazione di salute, psicologica, culturale e linguistica del paziente e proporzionata alla tipologia della prestazione proposta. L’informazione al paziente deve essere adeguata all’età (in caso di minorenne) ed alla condizione di capacità (nel caso di interdetto giudiziale o di incapace naturale). Per quanto possibile, va evitato il rischio di un involontario e non esplicito condizionamento, legato all’asimmetria informativa (chi sa e chi ignora) rispettivamente tra le figure del medico e del paziente, eventualmente accentuato dalla gravità della malattia e dalla complessità della terapia conseguente;
- Comprensibile: espressa con linguaggio semplice e chiaro, attraverso l’uso di:
- ▪ notizie e dati specialistici forniti senza ricorso a sigle o termini scientifici (qualora ritenuti indispensabili, essi devono essere accompagnati da spiegazione in lingua corrente);
- ▪ schede illustrate o materiale video che consentano al paziente di comprendere compiutamente ciò che verrà effettuato, soprattutto in previsione di interventi particolarmente invasivi o demolitivi;
- ▪ interprete o materiale informativo tradotto, ove possibile, in presenza di paziente straniero, affinché venga correttamente e completamente compreso ciò che viene detto; grafia leggibile per tipologia e dimensioni;
- Veritiera: ovvero non falsamente illusoria, ma prudente e accompagnata da ragionevole speranza nelle informazioni che hanno rilevanza tale da comportare gravi preoccupazioni o previsioni infauste;
- Obiettiva: basata su fonti validate o che godano di una legittimazione clinico - scientifica. Indicativa inoltre delle effettive potenzialità di cura fornite dalla struttura che ospita il paziente e delle prestazioni tecnico - strutturali che l’ente è in grado di offrire permanentemente o in quel momento;
- Esaustiva: Finalizzata a fornire le notizie inerenti all’atto sanitario proposto nell’ambito del percorso di cura intrapreso e al soddisfacimento di ogni quesito specifico posto dal paziente. In particolare, su:
- natura e scopo principale;
- probabilità di successo;
- modalità di effettuazione;
- sanitario che eseguirà la prestazione;
- conseguenze previste e loro modalità di risoluzione;
- rischi ragionevolmente prevedibili (complicanze), loro probabilità di verificarsi e di essere risolti da ulteriori trattamenti;
- eventuali possibilità di trattamenti alternativi, loro vantaggi e rischi;
- conseguenze del rifiuto alle prestazioni sanitarie.
- Non Imposta: Il paziente ha la facoltà di non essere informato, delegando a terzi la ricezione Non imposta delle informazioni, dal momento che il diritto all’informazione non necessariamente deve accompagnarsi all’obbligo di riceverla. Di questo deve tuttavia rimanere evidenza scritta. In tal caso egli esprimerà comunque il consenso, subordinatamente all’informazione data a persona da lui delegata.
12 http://www.agenziafarmaco.gov.it/content/cosa-sono-i-vaccini
13 https://www.ema.europa.eu/en/documents/product-information/comirnaty-epar-product-information_it.pdf
14 Si legge sul sito di Moderna alla voce “Our mRNA Platform” (https://www.modernatx.com/mrna-technology/mrna-platform-enabling-drug-discovery-development):
“Dobbiamo far entrare l'mRNA nei tessuti e nelle cellule bersaglio, eludendo il sistema immunitario. Se il sistema immunitario viene attivato, la risposta risultante può limitare la produzione di proteine e, quindi, limitare il beneficio terapeutico dei farmaci mRNA. Abbiamo anche bisogno che i ribosomi pensino che l'mRNA sia stato prodotto naturalmente, in modo che possano leggere accuratamente le istruzioni per produrre la giusta proteina. E dobbiamo anche assicurarci che la cellula produca abbastanza proteina da avere l'effetto terapeutico desiderato.”
15 vedi domanda-risposta AIFA n. 9, https://www.aifa.gov.it/documents/20142/1279946/FAQ-Vaccinazione_anti_COVID-19_con_vaccino_Pfizer.pdf/ea9099cd-c71c-d443-e447-6da60137da37
“Quanto dura la protezione indotta dal vaccino?
La durata della protezione non è ancora definita con certezza perché il periodo di osservazione è stato necessariamente di pochi mesi, ma le conoscenze sugli altri tipi di coronavirus indicano che la protezione dovrebbe essere di almeno 9-12 mesi.”
16 vedi domanda-risposta AIFA n. 11, https://www.aifa.gov.it/documents/20142/1279946/FAQ-Vaccinazione_anti_COVID-19_con_vaccino_Pfizer.pdf/ea9099cd-c71c-d443-e447-6da60137da37
“Le persone vaccinate posso trasmettere comunque l’infezione ad altre persone?
Gli studi clinici condotti finora hanno permesso di valutare l’efficacia del vaccino COVID-19 mRNA BNT162b2 (Comirnaty) sulle forme clinicamente manifeste di COVID-19 ed è necessario più tempo per ottenere dati significativi per dimostrare se i vaccinati si possono infettare in modo asintomatico e contagiare altre persone. Sebbene sia plausibile che la vaccinazione protegga dall’infezione, i vaccinati e le persone che sono in contatto con loro devono continuare ad adottare le misure di protezione anti COVID-19.”
https://palermo.repubblica.it/cronaca/2021/01/22/news/vaccinati-283710179/
https://www.lanazione.it/prato/cronaca/cresce-il-focolaio-al-santa-caterina-66-positivi-la-prima-dose-del-vaccino-solo-una-settimana-fa-1.5900472, https://www.lanazione.it/prato/cronaca/covid-vaccino-anziani-positivi-1.5902237
https://www.ilrestodelcarlino.it/cesena/cronaca/covid-focolaio-mercato-saraceno-1.5936567
https://www.today.it/attualita/anziani-morti-dopo-vaccino-covid-spagna.html
https://www.israelnationalnews.com/News/News.aspx/295582
https://www.israelnationalnews.com/News/News.aspx/294848
https://cnycentral.com/news/local/32-residents-die-from-outbreak-at-auburn-nursing-home
https://www.affaritaliani.it/coronavirus/vaccino-infermiere-positivo-dopo-ii-dose-sindacato-medici-non-panacea-723195.html
https://www.bresciatoday.it/attualita/coronavirus/vaccino-positivi.html
19 Long Term Care Community Coalition (LTCCC) fornisce un foglio di calcolo che tiene traccia dei decessi legati al COVID-19 nelle case di cura (NH) e nelle strutture di assistenza per adulti (ACF) di New York, sulla base dei dati del Dipartimento della Salute (DOH) di New York. Questo file, aggiornato ogni due settimane da LTCCC, include dati a livello di stato, contea e struttura. Dal 4 al 18 gennaio si registra un incremento di 561 morti rispetto alle due precedenti settimane e i dati oltretutto non includono i decessi COVID-19 confermati o COVID-19 presunti positivi avvenuti al di fuori della struttura, quando la media settimanale era di circa 16 decessi tra luglio e ottobre.
https://nursinghome411.org/wp-content/uploads/2021/01/nycovidfatality.01182021.xlsx
https://www.health.ny.gov/statistics/diseases/covid-19/fatalities_nursing_home_acf.pdf
21 Scrive lo scorso 4 gennaio sul BMJ: «Pfizer ha riportato 170 casi di covid-19 confermati da PCR, 8 nel gruppo vaccino e 162 nel gruppo placebo.
Tuttavia, questi numeri sono stati “sporcati” da una tipologia chiamata "sospetto covid-19", ovvero soggetti con sintomi riconducibili alla covid-19 non confermata da PCR. Secondo il rapporto della FDA sul vaccino della Pfizer, sul totale dei soggetti analizzati, sono stati rilevati "3410 casi totali di sospetto covid-19 non confermati, 1594 si sono verificati nel gruppo vaccino e 1816 nel gruppo placebo".
Essendo i casi sospetti 20 volte maggiori di quelli confermati, questa tipologia "sospetto covid-19” non può essere ignorata semplicemente perché non c'è stato un risultato positivo del test PCR. Anzi, per questo è ancora più urgente capire. Una stima approssimativa dell'efficacia del vaccino contro lo sviluppo di sintomi di covid-19, con o senza un risultato positivo del test PCR, rappresenterebbe una riduzione del rischio relativo del 19%, valore molto al di sotto della soglia di efficacia del 50% fissata dalle autorità di regolamentazione per l’autorizzazione. Anche dopo aver rimosso i casi verificatisi entro 7 giorni dalla vaccinazione (409 da vaccino Pfizer vs 287 da placebo), che dovrebbero includere la maggior parte dei sintomi dovuti alla reattogenicità del vaccino a breve termine, l’efficacia del vaccino resta bassa: 29%.»
22 Il richiedente potrà presentare dati aggiuntivi anche dopo l'autorizzazione all'immissione in commercio, contrariamente ad una normale autorizzazione all'immissione in commercio in cui tutti i dati sono presentati prima del rilascio dell’autorizzazione.
Il CMA (Conditional Marketing Approval) è valido per un anno, su base rinnovabile. L’Autorizzazione è subordinata alla presentazione, entro un periodo di tempo definito e a determinate scadenze, di ulteriori dati a supporto e consolidamento delle evidenze di efficacia e sicurezza (Specific Obligations - SOS), derivanti sia da studi ancora in corso al momento dell’autorizzazione per acquisire i risultati finali anche su nuovi endpoint, sia dando avvio a nuovi studi. La licenza può essere convertita in standard marketing authorization successivamente alla presentazione dei dati richiesti.
23 Le "revisioni a rotazione” consentono a EMA di valutare i dati non appena disponibili, invece di attendere la conclusione di tutte le sperimentazioni. Attraverso le revisioni a rotazione EMA valuta i dati mentre lo sviluppo è ancora in corso e prima che lo sviluppatore del vaccino presenti una richiesta di autorizzazione all'immissione in commercio.
26 https://www.fda.gov/vaccines-blood-biologics/vaccines/emergency-use-authorization-vaccines-explained
27 https://www.ft.com/content/12f7da5b-92c8-4050-bcea-e726b75eef4d
28 L’europarlamentare Stefania Zambelli lo scorso novembre ha presentato una Interrogazione con richiesta di risposta scritta alla Commissione (https://www.europarl.europa.eu/doceo/document/E-9-2020-006302_IT.pdf) rilevando che i contratti conclusi con le case farmaceutiche sono stati secretati dalla Commissione Europea e non se ne conosce l’entità economica, né si conoscono i prezzi dei vaccini, le tempistiche stimate per la produzione e distribuzione e le clausole di responsabilità applicate, né tantomeno l'identità dei negoziatori, chiedendo il motivo di tale segretezza.
29 https://ec.europa.eu/info/sites/info/files/curevac_-_redacted_advance_purchase_agreement_0.pdf
30 E più avanti alla voce “1.23. INDEMNIFICATION” si afferma:
“1.23.1. La Commissione, per conto degli Stati membri partecipanti, dichiara che l'uso del prodotto approvato nell'ambito del presente APA e/o dei Vaccine Order Forms avverrà in condizioni epidemiche (quindi condizioni particolari-eccezionali di epidemia) che ne richiedono tale uso, e che la gestione dei prodotti sarà quindi condotta sotto la sola responsabilità degli Stati membri partecipanti.
1.23.2. Le Parti dichiarano ulteriormente che le disposizioni contenute nella presente clausola d'indennizzo, comprese le eccezioni agli impegni d'indennizzo, riflettono le particolari circostanze della pandemia COVID- 19 e la necessità di sviluppare nuovi vaccini a una velocità senza precedenti per permettere un'immunizzazione su larga scala.”
L’europarlamentare Isabella Tovaglieri (https://www.facebook.com/IsabellaTovaglieriLega/videos/117341236919883) sottolinea come la Commissione Europea si stia comportando in spregio alle più elementari regole di trasparenza e democrazia secretando i contenuti dei contratti con i colossi farmaceutici con accordi per miliardi di euro. Dopo numerose richieste di accesso agli atti da parte dei parlamentari l’unico contratto reso accessibile è pieno di omissis nei passaggi chiave: “righe nere coprono infatti i dati sulla formulazione del vaccino, i dati sul costo delle fiale e soprattutto sulla responsabilità legale e finanziaria per gli effetti collaterali.
Questa totale mancanza di trasparenza stride particolarmente in quanto l'interesse pubblico dovrebbe prevalere sulla "riservatezza commerciale" durante una pandemia.
31 http://www.adrreports.eu/it/index.html
32 https://www.rtlnieuws.nl/sites/default/files/content/documents/2021/01/23/Beantwoording%20EMA.pdf
33 https://www.corriereromagna.it/ravenna-malore-improvviso-muore-farmacista-madre-di-4-figli/
34 Nel 2017, l’azienda biotecnologica tedesca CureVac ha pubblicato i risultati su The Lancet (vedi https://pubmed.ncbi.nlm.nih.gov/28754494/) per una sperimentazione di fase I del suo vaccino antirabbico mRNA e nel gennaio di quest'anno la società ha pubblicato i risultati tramite comunicato stampa (vedi https://www.curevac.com/en/2020/01/07/curevac-announces-positive-results-in-low-dose-1-%C2%B5g-rabies-vaccine-clinical-phase-1-study/) di uno studio di fase I del suo vaccino mRNA della rabbia a basso dosaggio.
Nel 2019, i ricercatori di Moderna e tedeschi hanno pubblicato i risultati di fase I di due vaccini a mRNA contro l’influenza (vedi https://www.sciencedirect.com/science/article/pii/S0264410X19305626).
A gennaio 2020, Moderna ha annunciato i risultati del suo studio di fase I su un vaccino a mRNA contro il citomegalovirus (vedi https://investors.modernatx.com/news-releases/news-release-details/moderna-announces-additional-positive-phase-1-data), e proprio lo scorso aprile, mentre infuriava la pandemia, la società ha riportato dati provvisori dal suo vaccino a mRNA contro Zika (vedi https://www.businesswire.com/news/home/20200414005276/en/Moderna-Highlights-Opportunity-mRNA-Vaccines-Vaccines-Day).
In un articolo su Nature Reviews Drug Discovery (vedi https://www.nature.com/articles/nrd.2017.243), Drew Weissman, MD, PhD, dell'Università della Pennsylvania a Philadelphia e uno dei primi pionieri della tecnologia dell'mRNA, e colleghi hanno scritto che i primi risultati dei vaccini con mRNA contro la rabbia e l'influenza "erano alquanto modesti, portando ad aspettative più caute sul passaggio dal successo preclinico alla clinica". Il team ha notato che in entrambi gli studi l'immunogenicità era "più modesta negli esseri umani di quanto ci si aspettasse sulla base di modelli animali, un fenomeno osservato anche con i vaccini a base di DNA, e gli effetti collaterali non erano banali".
35 vedi domanda-risposta AIFA n.18 (https://www.aifa.gov.it/documents/20142/1279946/FAQ-Vaccinazione_anti_COVID-19_con_vaccino_Pfizer.pdf/ea9099cd-c71c-d443-e447-6da60137da37)
“Chi ha già avuto un’infezione da Covid-19, confermata, deve o può vaccinarsi?
La vaccinazione non contrasta con una precedente infezione da COVID-19, anzi potenzia la sua memoria immunitaria, per cui non è utile alcun test prima della vaccinazione. Tuttavia, coloro che hanno avuto una diagnosi di positività a COVID-19 non necessitano di una vaccinazione nella prima fase della campagna vaccinale, mentre potrebbe essere considerata quando si otterranno dati sulla durata della protezione immunitaria.”
36 https://www.epicentro.iss.it/vaccini/covid-19-vaccino-pfizer-biontech, “I principali criteri di esclusione dallo studio sono stati una precedente positività al COVID-19, il trattamento con immunosoppressori o una patologia del sistema immunitario.”
«A sottolineare l’importanza di questo sottogruppo di “guariti Covid” è proprio Massimo Galli: “Nessun dato scientifico sostiene la immediata necessità e la sicurezza del vaccino nel loro caso. Nei guariti non va quindi praticato almeno fino a che non ne sapremo di più. Per rendere le cose comode e non porci il problema di capire chi si sta vaccinando, (se è già stato infettato oppure no), facciamo dei disastri”.»
37 https://www.ema.europa.eu/en/documents/product-information/comirnaty-epar-product-information_it.pdf
38 https://www.ema.europa.eu/en/documents/rmp/comirnaty-epar-risk-management-plan_en.pdf
40 https://doi.org/10.1016/j.addr.2020.07.024
41 Gergely Tibor Kozma, Taro Shimizuc, Tatsuhiro Ishida, Janos Szebeni (2020). Anti-PEG antibodies: Properties, formation, testing and role in adverse immune reactions to PEGylated nano-biopharmaceuticals. https://doi.org/10.1016/j.addr.2020.07.024
https://www.sciencedirect.com/science/article/pii/S0169409X20301083
Moreno, A., Pitoc, G., Ganson, N., Layzer, J., Hershfield, M., Tarantal, A. and Sullenger, B. (2019). Anti-PEG Antibodies Inhibit the Anticoagulant Activity of PEGylated Aptamers. Cell Chemical Biology, 26(5), pp.634-644.e3. www.cell.com/cell-chemical-biology/pdfExtended/S2451-9456(19)30035-2
Neun, B., Barenholz, Y., Szebeni, J. and Dobrovolskaia, M. (2018). Understanding the Role of Anti-PEG Antibodies in the Complement Activation by Doxil in Vitro. Molecules, 23(7), p.1700. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6100003/
Zhang, P., Sun, F., Liu, S. and Jiang, S. (2016). Anti-PEG antibodies in the clinic: Current issues and beyond PEGylation. Journal of Controlled Release, 244, pp.184-193. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5747248/
45 Secondo uno studio promosso dai Centers for Disease Control and Prevention degli Stati Uniti e pubblicato nel 2015 (https://www.aifa.gov.it/-/vaccini-causano-molto-raramente-anafilassi-uno-studio-del-cdc; https://www.sciencedirect.com/science/article/abs/pii/S0091674915011604) , la vaccinazione scatena molto raramente l’anafilassi: il tasso di anafilassi è risultato pari a 1.31 casi per milione di dosi, ovvero il ricercatori hanno identificato 33 casi confermati di anafilassi innescata dal vaccino che si sono verificati a seguito della somministrazione di 25.173.965 dosi di vaccino analizzando tutti i dati riferiti a tre anni (da gennaio 2009 a dicembre 2011).
Dalle evidenze disponibili il rischio che Comirnaty possa innescare l’anafilassi o gravi reazioni allergiche appare ben oltre la soglia osservata per altri vaccini.
48 Non esiste una definizione uniformemente accettata di VAED o VAERD. I termini correlati utilizzati di frequente includono "malattia potenziata mediata dal vaccino (VMED)", "malattia respiratoria potenziata (ERD)", "potenziamento dell'infezione indotta dal vaccino", "potenziamento della malattia", "potenziamento delle difese immunitarie" e "potenziamento degli anticorpi dipendenti (ADE)”. Ciò potrebbe rendere problematica la comparabilità dei dati tra gli studi o dei dati raccolti attraverso i sistemi di sorveglianza se non viene utilizzata una definizione coerente dei casi. Vedi https://brightoncollaboration.us/wp-content/uploads/2020/10/JVAC-S-20-02520_mzd.pdf
49 Vedi domanda-risposta AIFA n. 9,
https://www.aifa.gov.it/documents/20142/1279946/FAQ-Vaccinazione_anti_COVID-19_con_vaccino_Pfizer.pdf/ea9099cd-c71c-d443-e447-6da60137da37
“Quanto dura la protezione indotta dal vaccino?
La durata della protezione non èncora definita con certezza perché il periodo di osservazione ètato necessariamente di pochi mesi, ma le conoscenze sugli altri tipi di coronavirus indicano che la protezione dovrebbe essere di almeno 9-12 mesi.”
50 Timothy Cardozo, Ronald Veazey (2020). Informed consent disclosure to vaccine trial subjects of risk of COVID‐19 vaccines worsening clinical disease. https://doi.org/10.1111/ijcp.13795
https://onlinelibrary.wiley.com/doi/10.1111/ijcp.13795
52 https://govextra.gov.il/media/30806/11221-moh-pfizer-collaboration-agreement-redacted.pdf
53 https://www.fda.gov/media/144413/download
54 https://eur-lex.europa.eu/legal-content/IT/TXT/HTML/?uri=CELEX:52020DC0245&from=EN, https://www.europarl.europa.eu/news/it/press-room/20200706IPR82731/covid-19-il-parlamento-deve-consentire-uno-sviluppo-piu-rapido-dei-vaccini#:~:text=La%20Commissione%20ha%20proposto%20un,o%20sono%20costituiti%20da%20OGM.,
https://data.consilium.europa.eu/doc/document/PE-28-2020-INIT/en/pdf
“La direttiva 2009/41/CE stabilisce che i rischi per la salute umana e l'ambiente associati all'impiego confinato di microrganismi geneticamente modificati devono essere valutati caso per caso. A tal fine, la direttiva prevede che l'utilizzatore valuti i rischi per la salute umana e per l'ambiente che il tipo specifico di impiego confinato può comportare, utilizzando come minimo gli elementi di valutazione e la procedura di cui all'allegato III di tale direttiva.”
https://apnews.com/article/virus-outbreak-archive-united-nations-54a3a5869c9ae4ee623497691e796083
58 http://www.dmi.unipg.it/mamone/sci-dem/scidem.htm
59 https://www.istat.it/it/files//2020/12/Rapp_Istat_Iss.pdf
60 https://www.istat.it/it/files//2020/03/morti-gennaio-novembre-2015-2020.xlsx
61 https://www.istat.it/it/archivio/240401
62 https://www.epicentro.iss.it/coronavirus/bollettino/Report-COVID-2019_16_dicembre.pdf
63 https://www.quotidianosanita.it/cronache/articolo.php?articolo_id=91530
65 Il professor Stefano Petti, intervistato dalla giornalista Gioia Locati, ha evidenziato questo significativo aspetto consultando le tabelle divulgate dell’Office of National Statistics inglese che mostrano l’andamento dei decessi del dicembre 2020 in Inghilterra e quello degli anni precedenti: nel 2020 i decessi Covid compaiono al primo posto.
Al secondo le morti per demenza, al terzo gli infarti, al quarto gli ictus. In Italia simili dati non sono disponibili, ma è facilmente deducibile che la situazione si presenti parimenti.
“Da un confronto con la media dei 5 anni precedenti osserviamo che nel 2020 i decessi per infarto sono scesi del 6%, quelli per demenza dell’11%, quelli per ictus (cerebrovascular diseases) del 12%. Perfino le morti da tumore si sono ridotte: le neoplasie polmoni-trachea-bronchi si sono ridotte del 7%, mentre la mortalità per influenza si è pressoché dimezzata, -50% …
66 http://www.quotidianosanita.it/scienza-e-farmaci/articolo.php?articolo_id=91683
68 https://www.agi.it/cronaca/news/2021-01-11/primo-caso-covid-italia-novembre-2019-10978766/ ; https://www.adnkronos.com/coronavirus-studio-italiano-epidemia-nata-tra-ottobre-e-novembre-2019_2omDlr9YR2yXfsq6JtBEKF ; https://www.repubblica.it/cronaca/2020/02/28/news/coronavirus_studio_italiano_all_oms_epidemia_da_ottobre_contagi_raddoppiati_ogni_4_giorni-249808885/
71 https://www.epicentro.iss.it/coronavirus/bollettino/Report-COVID-2019_16_dicembre.pdf
72 https://www.indexmundi.com/g/g.aspx?c=it&v=26&l=it
75 https://www.eea.europa.eu//publications/air-quality-in-europe-2020-report
76 https://www.epicentro.iss.it/ambiente/AriaEuropa2015
77 https://www.dailymail.co.uk/health/article-8875201/Has-Covid-killed-flu.html
78 https://www.epicentro.iss.it/influenza/flunews#epi
79 https://w3.iss.it/site/RMI/influnet/pagine/rapportoInflunet.asp
82 https://www.lanuovabq.it/it/medici-di-base-impotenti-ma-ho-continuato-a-curare
83 https://www.quotidianosanita.it/cronache/articolo.php?articolo_id=91530
85 Nella circolare viene fornita la definizione di caso lieve:
“Per caso lieve si intende: presenza di sintomi come febbre (>37.5°C), malessere, tosse, faringodinia, congestione nasale, cefalea, mialgie, diarrea, anosmia, disgeusia, in assenza di dispnea, disidratazione, alterazione dello stato di coscienza.”
Si legge: “In linea generale, per soggetti con queste caratteristiche cliniche non è indicata alcuna terapia al di fuori di una eventuale terapia sintomatica di supporto. In particolare, nei soggetti a domicilio asintomatici o paucisintomatici, sulla base delle informazioni e dei dati attualmente disponibili, si forniscono le seguenti indicazioni di gestione clinica:
- vigile attesa;
- misurazione periodica della saturazione dell’ossigeno tramite pulsossimetria;
- trattamenti sintomatici (ad esempio paracetamolo);
- appropriate idratazione e nutrizione;
- non modificare terapie croniche in atto per altre patologie (es. terapie antiipertensive, ipolipemizzanti, anticoagulanti o antiaggreganti), in quanto si rischierebbe di provocare aggravamenti di condizioni preesistenti;
- i soggetti in trattamento immunosoppressivo cronico in ragione di un precedente trapianto di organo solido piuttosto che per malattie a patogenesi immunomediata, potranno proseguire il trattamento farmacologico in corso a meno di diversa indicazione da parte dello specialista curante;
- non utilizzare routinariamente corticosteroidi;
- l’uso dei corticosteroidi è raccomandato nei soggetti con malattia COVID-19 grave che necessitano di supplementazione di ossigeno. L’impiego di tali farmaci a domicilio può essere considerato solo in quei pazienti il cui quadro clinico non migliora entro le 72 ore, in presenza di un peggioramento dei parametri pulsossimetrici che richieda l’ossigenoterapia;
- non utilizzare eparina. L’uso di tale farmaco è indicato solo nei soggetti immobilizzati per l’infezione in atto;
- non utilizzare antibiotici. Il loro eventuale uso è da riservare solo in presenza di sintomatologia febbrile persistente per oltre 72 ore o ogni qualvolta in cui il quadro clinico ponga il fondato sospetto di una sovrapposizione batterica, o, infine, quando l’infezione batterica è dimostrata da un esame microbiologico;
- non utilizzare idrossiclorochina la cui efficacia non è stata confermata in nessuno degli studi clinici controllati fino ad ora condotti;
- non somministrare farmaci mediante aerosol se in isolamento con altri conviventi per il rischio di diffusione del virus nell’ambiente.”
È evidente che le cure, nella primissima fase della malattia, possono contribuire a bloccare il virus o limitare fortemente l’evoluzione verso forme gravi. E oggi, purtroppo, mancano ancora linee guida uniformi per il trattamento domiciliare del coronavirus in fase precoce.
88 Continua il Dott. Cosentino:
“La malattia è subdola, con andamento variabile da persona a persona e con remissioni che purtroppo in alcuni casi preludono a repentini aggravamenti. Per questo è estremamente importante che il medico segua con assiduità e attenzione i propri assistiti fin dai primi sintomi, pronto a somministrare le terapie più appropriate in relazione al quadro clinico.”
(…)
“Indubbiamente, tra gli aspetti singolari e incomprensibili che ancora osserviamo, a quasi un anno di distanza dai primi casi di Covid, va annoverata anche la resistenza a considerare l’esperienza acquisita “sul campo” da tanti medici che hanno curato e continuano a curare le persone con successo, riducendo al minimo il numero di casi che si aggrava al punto da rendere necessario il ricovero, e realizzando in tal modo il miglior beneficio per i loro pazienti e al tempo stesso per il sistema sanitario.”
(…)
“Suggerire il paracetamolo per ridurre la febbre è senza dubbio una scelta singolare. Tra i farmaci antiinfiammatori non steroidei, i cosiddetti FANS, categoria cui il paracetamolo appartiene, esso è l’unico ad essere – come gli altri FANS – antipiretico e analgesico ma – a differenza degli altri FANS – privo di significativa attività antiinfiammatoria. I fenomeni infiammatori sono peculiari del Covid fin dagli esordi, ed esistono studi quanto meno di natura osservazionale che descrivono un’evoluzione nettamente più favorevole nei pazienti Covid in trattamento con aspirina, il capostipite dei FANS, antiinfiammatorio per antonomasia. Semmai, l’eventuale preoccupazione per i possibili disturbi che l’aspirina potrebbe causare nel tratto gastrointestinale potrebbe suggerire di ricorrere ad altri FANS comunque antiinfiammatori quali l’ibuprofene o il ketoprofene, meglio tollerati a quel livello. Esiste poi un comune consenso sul beneficio nel Covid a un certo stadio derivante dalla riduzione dell’aggregazione piastrinica e in generale della coagulazione. Tutti i FANS sono anche antiaggreganti piastrinici, ancora una volta tuttavia con l’eccezione del paracetamolo. Difficile quindi difendere la decisione di indicare il paracetamolo come FANS di scelta”.
(…)
AIFA arrivò a pubblicare una nota che vietava l’uso di idrossiclorochina, interferendo in tal modo sul diritto esclusivo e inviolabile dei medici di prescrivere quelle cure che, “in scienza e coscienza”, siano ritenute nel migliore interesse del paziente. Su questo aspetto il Consiglio di Stato si è pronunciato, arrivando a definire “irragionevole” la sospensione dell’uso del farmaco. Si tratta di una sentenza severa, che utilizza espressioni pesanti per stigmatizzare una decisione indubbiamente singolare dell’ente regolatorio. Purtroppo la discussione intorno all’idrossiclorochina, così come su altri rimedi di efficacia più che probabile – come ad esempio il plasma convalescente – è stata inquinata da connotati di natura politica, che nulla hanno a che fare con la medicina.”
(…)
In assenza di linee guida efficaci riguardo alle terapie domiciliari, sono nate significative iniziative allo scopo di condividere esperienze, pareri e buone pratiche, contribuendo così a salvare più vite possibili. Fra queste:
- Il Dott. Andrea Mangiagalli nel marzo scorso ha dato vita ad una iniziativa con la dottoressa Laura Frosali che raccoglie circa duecento medici.
“Il principale problema di questa pandemia è che la Medicina di base è stata considerata residuale e così il medico è stato prima tenuto ai margini o costretto ad autoescludersi dalla cura del covid e poi abbandonato senza strumenti. Invece la risposta migliore che si può dare alla pandemia sta proprio nel nostro lavoro tempestivo e nella precocità di intervento terapeutico. I risultati sono strabilianti, a cominciare dal fatto che i nostri pazienti non sono mai stati ricoverati”. Così spiega il Dott. Mangiagalli in un’intervista alla Nuova Bussola Quotidiana (https://www.lanuovabq.it/it/cosi-con-una-chat-e-la-clorochina-battiamo-il-covid). - Il Movimento Ippocrate (https://ippocrateorg.org/2020/11/26/come-si-affronta-il-covid-19/ ; https://www.farodiroma.it/terapie-alternative-che-funzionano-il-dottor-stramezzi-che-ha-guarito-160-pazienti-affetti-da-covid-19/) raggruppa una rete internazionale di Medici, Ricercatori, Operatori della Sanità, Operatori nel Sociale; propone “dettagliate linee guida, con specifica di farmaci, posologie e tempistiche, nella speranza che chi ha l’onere di dover produrre delle indicazioni precise per la cittadinanza si decida a farlo oppure lasci il proprio posto a persone più adeguate a gestire questa crisi” come si può leggere nel sito.
- Il gruppo Facebook #Terapiadomiciliarecovid19 (https://www.facebook.com/groups/273910870288111) creato dall’avvocato del foro di Napoli Erich Grimaldi che raccoglie oggi più di 65.000 iscritti con l’obiettivo di per far dialogare i medici dei territori sulle terapie anti Covid, condividere le esperienze e le buone pratiche e contribuire così a salvare più vite possibili.
- Il “Comitato per il diritto alla cura tempestiva domiciliare nell’epidemia di Covid” (https://www.terapiadomiciliarecovid19.org/) di cui l’avv. Grimaldi è fondatore e presidente.
- Il professore Luigi Cavanna, direttore del dipartimento di oncoematologia dell'ospedale di Piacenza, durante il picco dell'epidemia, nei mesi di marzo e aprile, ha curato centinaia di pazienti recandosi presso le loro abitazioni. La sua testimonianza ha persino attirato l’attenzione di una rivista settimanale di notizie tra le più diffuse nel mondo, vedi https://time.com/5816874/italy-coronavirus-patients-treating-home/
- Il professor Piero Sestili, Ordinario di Farmacologia dell’Università di Urbino e la Dott.ssa Roberta Ricciardi, responsabile del Percorso Miastenia dell'Ospedale Cisanello di Pisa, sono fra i circa 50 firmatari di un appello lanciato ad AIFA e al ministero lo scorso aprile per usare il cortisone nelle prime fasi della malattia da coronavirus, associandolo a una terapia antibiotica di copertura e a un trattamento anticoagulante. (vedi https://www.ilgiornale.it/news/cronache/questa-terapia-cura-covid-ministro-non-ha-risposto-1868947.html)
- In un’intervista pubblicata lo scorso 4 febbraio da “Il Resto del Carlino” il Prof. Sestili dichiara di aspettarsi che AIFA con la nuova gestione del presidente Giorgio Palù approvi e diffonda le linee guida per curarsi da casa. Se fosse stato accolto il loro approccio terapeutico si "Poteva risparmiare vittime, ricoveri, terapie intensive sia nella coda delle prima ondata sia nella seconda fase della malattia dopo l’estate".
(vedi https://www.ilrestodelcarlino.it/pesaro/cronaca/covid-la-terapia-a-casa-poteva-salvare-tante-vite-1.5982456)
Sulla necessità immediata di una guida alla gestione degli approcci terapeutici domiciliari nel contesto di un diffuso consumo di risorse ospedaliere, morbilità e mortalità, si segnala anche la pubblicazione Peter A. McCullough, Ronan J. Kelly, Gaetano Ruocco, Edgar Lerma, James Tumlin, Kevin R. Wheelan, Nevin Katz, Norman E. Lepor, Kris Vijay, Harvey Carter, Bhupinder Singh, Sean P. McCullough, Brijesh K. Bhambi, Alberto Palazzuoli, Gaetano M. De Ferrari, Gregory P. Milligan, Taimur Safder, Kristen M. Tecson, Dee Dee Wang, John E. McKinnon, William W. O'Neill, Marcus Zervos, Harvey A. Risch, Pathophysiological Basis and Rationale for Early Outpatient Treatment of SARS-CoV-2 (COVID-19) Infection, The American Journal of Medicine, Volume 134, Issue 1, 2021, Pages 16-22, ISSN 0002-9343, https://doi.org/10.1016/j.amjmed.2020.07.003 https://www.sciencedirect.com/science/article/pii/S0002934320306732
Dalle testimonianze di medici e di pazienti (Fuori dal coro: Puntata del 26 gennaio: https://www.mediasetplay.mediaset.it/video/fuoridalcoro/virus-noi-pazienti-curati-in-casa_F310754201003C27 ; Fuori dal coro: Puntata del 20 gennaio: https://www.mediasetplay.mediaset.it/video/fuoridalcoro/covid-e-terapie-in-casa-la-parola-dei-medici-di-base_F310754201002C32), si apprende che la Covid-19 può essere curata a casa con successo anche nel caso in cui colpisse soggetti cosiddetti fragili.
89 https://www.tg24.info/focus-covid-da-reggio-calabria-la-terapia-sperimentale-contro-il-virus-bocciata-da-aifa/ ; https://opinione.it/societa/2021/01/11/vanessa-seffer_covid-adenosina-pandemia-correale-macheda-gom-atp-polmoni-aifa-vaccino/






